الصبغي (الكروموزوم)
الصبغي (الكروموزوم) chromosome، جسيم مجهري خيطي الشكل كثير الالتفاف، تترتب الجينات (المورثات) genes على امتداده، وقد اشتقت كلمة كروموزوم من كلمتين يونانيتين هما Chromo (لون) وsoma(جسم)، لأن الصبغي يمكن تلوينه بأصبغة معينة.
يُعد العالم الألماني والتر فليمنغ(1843ـ1905) Walter Flemming مؤسس علم الوراثة الخلوية، أول من درس ووصف سلوك الصبغيات ضمن نواة الخلية في أثناء الانقسام الخلوي العادي (الخيطي أو الفتيلي)mitosis. ففي عام 1879 لاحظ فليمنغ أن بعض أصبغة الأنوية الخلوية أظهر فيها مادة خيطية الشكل. فاستخدم تلك الأصبغة في خلايا تم «قتلها» في مراحل مختلفة من الانقسام، ولاحظ سلسلة من التغيرات تحدث ضمن الأنوية، وأوضح أن تلك «الخيوط»، التي أسماها فلهيلم فون فولدير Wilhelm von Waldeyer «كرموزومات» (صبغيات)، قد قصرت أطوالها وانشطرت طولياً إلى أنصاف، توجه كل نصف منها إلى أحد قطبي الخلية. وأطلق فليمنغ على هذه العملية اسم الانقسام العادي (الخيطي أو الفتيلي) ووصفها عام 1882 في كتابه المهم «المادة الخلوية، النواة، والانقسام الخلوي» Zell-substanz, Kern und Zelltheilung ولم تُعرّف أهمية دراساته في مجالات الوراثة إلا بعد اكتشاف قوانين مندل[ر] بعد نحو عقدين من الزمن.
تطورت دراسات الانقسام الخلوي وسلوك الصبغيات منذ النصف الثاني من القرن التاسع عشر، وفي عام 1900، أعيد اكتشاف قوانين مندل من قبل كورينسCorrens وتشيرماك Tschermakودوفريس De Vries، بعد تجاهلها نحو 35سنة. وفي عام 1903، قدم ساتونW.S.Sutton التفسير الواضح الأول للعلاقة بين «العوامل» الوراثية التي اقترحها مندل (وأُسميت فيما بعد الجينات genes «أو المُوَرِّثات») وبين الصبغيات. وتتابعت أبحاث واكتشافات باهرة في القرن العشرين الذي يمكن تسميته قرن الثورة الوراثية، ولاشك أن أبرزها كان اكتشاف واطسون Watsonوكريك Crick عام 1953 التركيب الحلزوني المضاعف للحمض الريبي النووي المنقوص الأكسجين deoxyribonucleic acid (الدناDNA).
بنية الصبغي
في معظم حياة الخلية تصعب مشاهدة الصبغيات مجهرياً منفردة لصغرها وَرِقَّتِها والتفافها، فإذا ماصبغت ودرست مجهرياً فإن النواة تُشاهد عادة على شكل مناطق ملونة فاتحة وأخرى داكنة. أما في أثناء الانقسام الخلوي فإن الصبغيات تتكثف على هيئة عُضَيّات organelles صغيرة محددة يمكن صبغها، وبالتالي مشاهدتها بالمجهر الضوئي العادي. وفي أثناء المرحلة المسماة مرحلة Sيشاهد كل صبغي مشطوراً طولياً إلى مُكَوِّنَيْن متماثلين يدعى كل منهما كروماتيدchromatid.
الصبغيات جسيمات بالغة الدقة والالتفاف (الشكل 1)، تتألف من الحمض الريبي النووي المنقوص الأكسجين (الدناDNA)، ولو أمكن فَرْدُ دنا صبغيات خلية إنسانية واحدة ووصلت فيما بينها لبلغ طولها نحو المترين. وبهذه الالتفافات تتمكن النواة، التي لايتجاوز قطر الخلية التي تحويها نحو 6ميكرومتر، من احتواء دنا الصبغيات الستة والأربعين الخاصة بالإنسان، ويحقق ذلك عدة مستويات من الالتفاف coiling، بمساعدة بروتينات الكروماتين، مما يؤدي إلى إنقاص حجم الصبغي نحو 8آلاف مرة عما هو عليه في الدور البيني interphase. ويُراوح طول جزيء الدنا في الصبغي البشري بين نحو 50×10 6زوج من النيوكليوتيدات في أصغر صبغي (يبلغ طوله إذا فُرِد نحو 1.7سم) و نحو 250×10 6زوج منها في أطول صبغي (يبلغ طوله إذا فُرد نحو 8.5سم).
يجتمع الكروماتيدان معاً بوساطة القسيم المركزي centromere الذي يحتوي على نحو مليون زوج من القواعد (BP) base pairs في الخلية الإنسانية، غالبيتها تتالياتrepetitive من الدنا، تتكرر ترادفياً (الواحدة بعد الأخرى) مرات ومرات. يعطي القسيم المركزي كل صبغي شكله المميز، ويمكن استخدامه للمساعدة في تحديد مواقع بعض المورثات. ويختلف موقعه من صبغي إلى آخر، فهو إما مركزي metacentric، أو قريب من المركز submetacentric، أو طرفيacrocentric، أوانتهائي telocentric (الشكل 2).
تتكون البروتينات عند القسيم المركزي مشكلة نقاط ارتباط الكروماتيدات مع الخيوط المغزلية (الشكل 3) في أثناء الدور الثاني (الاستوائي) من الانقسام الخيطي، أو الصبغيات في الانقسام المنصف، لترحل في الدور الثالث نحو قطبي الخلية.
الدنا هو المادة الوراثية في الكائنات الحية، وتمتلك كل خلية في جسم الفرد من نوع معين الدنا ذاته (إلا في حال حدوث طفرات أو شذوذ صبغي). وتتركز غالبية الدنا ضمن أنوية الخلايا، بينما تحتوي المتقدرات (الميتوكوندريا) mitochondria على كميات قليلة منه. ويخزِّن الدنا التعليمات الوراثية بشكل مرمَّز coded من أربعة حروف يمثل كل منها اسم قاعدة هي: الأدينين adenine (A)والغوانين guanine (G) والسيتوزين cytosine (C) والثيمين thymine (T). ويتكون دنا الإنسان من نحو 3مليار قاعدة، أكثر من 99% منها متماثل في كل البشر. وتعمل تتاليات القواعد على تحديد البيانات التي ستستخدم لبناء الكائن الحي والمحافظة عليه. ويوضح الجدول (1) اختلاف أعداد القواعد في بعض الصبغيات.
تقترن أزواج القواعد معاً، A مع T، وCمع G بروابط هدروجينية، وتتصل كل قاعدة آزوتية مع جزيء سكر (ريبوز منقوص الأكسجين deoxyribose)، وهذا مع فسفات لتكوين مايدعى نَوَويد (نوكليوتيد)nucleotide (الشكل ـ4). وتترتب النوويدات في «جديلتين» طويلتين لتكوين اللولب المزدوج double helix الذي يشبه سلَّماً «درجاته» أزواج القواعد الآزوتية، وجانباه جزيئات السكر والفسفات (الشكل ـ 4).
تحتوي الصبغيات على الغالبية العظمى من الجينات، ويستثنى من ذلك العدد الضئيل منها في المتقدرات، والضروري لتكوين مركب ثالث فسفات الأدينوزين adenosine triphosphate (ATP) الغني بالطاقة، وفي الصانعات الخضر chloroplasts الضرورية لعملية التركيب الضوئي photosynthesis.
وفي الكائنات الحقيقية النواةeukaryotes، يتألف الصبغي من سلسلة طويلة مفردة من الدنا DNA، مرتبطة بنسخ كثيرة من خمسة أنواع من الهستونات histones (H1, H2a, H2b, H3, H4 بنسب 1:2:2:2:2)، وهي بروتينات تدعم تركيب الصبغي، غنية بالليسين lysine والأرجينين arginine، وتمتلك بالتالي شحنة موجبة تمكنها من الترابط مع فوسفات الدنا ذات الشحنة السالبة.
تقوم الهستونات بدور مهم في تكثيف الدنا ضمن الصبغيات، ويمكن باستخدام المجهر الإلكتروني مشاهدة حبات beadsقطر كل منها نحو 100أنغستروم مرتبة على صبغي سبق أن عومل بمنظفات detergentsمعينة، تدعى النوكليوزومات nucleosomes، تتكون من الدنا ونسختين من كل من الهستونات H2a, H2b, H3, H4، ويلتف نحو 200زوج من القواعد حولها مرتين، أما الهستون H1 فإنه يكون بين النوكليوزيدات على الدنا (الشكل 5)، فيحقق ذلك تكثيفاً أشد للدنا. ويبلغ قصر الصبغي حده الأقصى في الطورين الثاني metaphase والثالثanaphase من الانقسام الخلوي.
يضاف إلى ذلك عدد قليل من النسخ من عدة أنواع من البروتينات غير الهستونية، معظمها عوامل انتساخ transcription factorsتنظم أجزاء الدنا التي سوف يتم انتساخها إلى حمض ريبي نووي ribonucleic acid (رناRNA)، وتعمل هذه البروتينات على ضغط النيوكليوسومات أكثر بشكل لفّات مدمجة.
أما في الكائنات البدائية النواةprokaryotes، كالبكتريا، فإن الصبغي يتألف من دنا حلقي غير محاط بغلاف نووي (الشكل 6).
يطلق على المعقد المكوَّن من الحموض النووية (DNA وRNA) والبروتينات اسم الكروماتين chromatin. ويقسم إلى نوعين:
1ـ الكروماتين السوي euchromatin: وهو جزء الصبغي الذي لايقبل الصبغ أو يقبله قليلاً، ويعتقد أنه يحوي الجينات الفعالة، ويشاهد في الخلايا النشيطة. وإن وجود هذا الكروماتين مهم لحاجة المناطق التي ستُستنسخ أو تتضاعف إلى فك الالتفاف قبل أن يمكن قراءة الشفرة الوراثية.
2ـ الكروماتين المتغاير heterochromatin: وهو كروماتين مكثف يقبل الصبغ بشدة، ويعتقد أن معظمه خامل وراثياً. يظل هذا الكروماتين ملتفاً بشدة خلال الدورة الخلوية، ويُشاهد في بعض الأحيان مجاوراً للغلاف النووي، ولكنه يكون آنذاك مقطعاً بمناطق فاتحة عند مسام pores الغلاف المذكور، مما يُسهل عمليات التبادل بين النواة والهيولى (السيتوبلازم).
الأعداد الصبغية
لكل كائن حي عدد ضعفاني (مضاعف)2n)ء) diploidمن الصبغيات في خلاياه، كل اثنين منها متماثلان، مصدر أحدهما الأب والثاني الأم، وصلا إلى النسل عبر الأعراس المذكرة والمؤنثة، التي تمتلك أعداداً فردانيةhaploid (n) من الصبغيات. ويبين الجدول (2) الأعداد الصبغية الضعفانية في عدد من الأنواع.
ومن جهة أخرى، فإن الصبغيات تصنَّف في مجموعتين:
ـ الصبغيات الجسمية (A)autosomes، التي لاتختلف بين الذكور والإناث.
ـ صبغيا الجنس sex chromosomes، وهما متماثلان في إناث الثدييات، يرمز لكل منهما بـ X، ومختلفان في ذكورها، حيث يكون أحدهما X والثاني أصغر حجماً ويرمز له بـ Y، وعلى هذا تكون الصيغة الصبغية للرجل 44A+XY وللمرأة 44A+X.
تشترك جميع الكائنات الحقيقية النواة التي تمت دراستها بكون صبغياتها ضعفانية العدد، لاتقل عن اثنين، وبامتلاكها دنا خيطي الشكل. والاختلاف الرئيس بينها هو في عدد الصبغيات، ويبدو أن هذا العدد ليس مرتبطاً بالصفات الحيوية للنوع، فمثلاً، يوجدفي الخميرة 16صبغياً، أي أربعة أضعاف ماتمتلكه ذبابة الخل[ر]. كما أن عدد الصبغيات ليس مرهوناً بحجم الجينوم، فمثلاً يوجد في بعض أنواع السلمندل salamanderجينوماً يزيد على ما يحوي في جينوم الإنسان بنحو 30مرة، ولكن عدد صبغياتها نصف عدد صبغيات الإنسان. ومع أهمية هذه الملاحظات، فإنها لاتدل إلا على عدم التجانس في عمليات التطور التي أدت إلى تحديد الأعداد الصبغية والجينومات في الأنواع المختلفة.
تعيين موقع الجين على الصبغي
يمتلك الفرد أعداداً كبيرة من الجينات (المورثات)، مرتبة طولياً على أجسام الصبغيات، وقد أمكن تحديد جميع القواعد في صبغيات الإنسان البالغة 46 صبغياً، وهو ماحققه مشروع الجينوم البشري [ر] Human Genome Project.
لكل جين موقع خاص به على صبغي معين، ويمكن تحديده بكتابته كموقع محدد:s17q12، أوبين حدين (مدى) إذا لم يكن الموقع محدداً بدقة: s17q12-q21.
توفر الأعداد والحروف بهذه الطريقة «عنواناً» لموقع كل جين على صبغي. ويتألف هذا العنوان من الآتي:
ـ رقم الصبغي الذي يوجد الجين فيه، وهو 17 في المثالين السابقين. وتمثل الصبغيات الجسمية 1ـ22 بأرقامها، أما الصبغيان الجنسيان فيشار إليهما بـ X أو Y.
ـ يقسم الصبغي إلى ذراعين، يدعى القصير منهما p والطويل q. ورمز الذراع هو الجزء الثاني من عنوان الجين، إذ يلي رقم الصبغي مباشرة. فمثلاً 7q هي الذراع الطويل من الصبغي السابع، بينما Xp هي الذراع القصير من الصبغي X.
ـ موقع الجين على الذراع القصير أو الطويل. ويزداد هذا الرقم مع ازدياد بعد الجين عن القسيم المركزي. وقد بُنيَ الموقع الدقيق للجين على نظام العصيبات bandsالداكنة والفاتحة التي تميز الصبغي وتظهر بعد الصبغ (الشكل 7). ويكون ذلك باستخدام رقمين: أولهما هو رمز المنطقةregion، وثانيهما رمز العصيبة، وقد يُتبعان بفاصلة عشرية يليها رقم أو أكثر (تمثل أجزاء العصيبات sub-bands ضمن منطقة داكنة أو فاتحة).
ـ وقد يضاف أحياناً أحد المقطعين terأو cen للإشارة إلى أن المورثة قريبة جداً من القسيم المركزي، مثلاً: 16pcen، أو أنه قريب جداً من نهاية الذراع، مثلاً: 14 qter، أو يستخدم المقطع tel للإشارة إلى أن الجين موجود في التيلومير في نهاية الذراع.
تضاعف الدنا DNA Replication
الانقسامات الخلوية عملية معقدة ومهمة تمكن الكائن الحي من النمو في المراحل الأولى من عمره، ومن تكوين خلايا تعوِّض الخلايا التالفة أو المعمرة. وتسمح الصبغيات للدنا بأن يعيد إنتاج ذاته (الشكل 8)، وبالتالي فإن كلاً من الخليتين البنتين الناتجتين من الانقسام الخلوي تحتوي على جميع الجينات الموجودة في الخلية الأم.
للصبغيات قدرة كبيرة على تغيير أشكالها وأحجامها إبان الدورة الخلوية. ففي الطور البيني interphase من هذه الدورة، وهي الأطول، فإن دنا الجينات النشيطة يكون معرضاً لتأثير الأنزيمات الضرورية لاصطناع الحمض الريبي النووي (الرنا RNA)، وكذلك في مرحلة تضاعف الدنا والتي تشمل جزيء الدنا بكامله، والمسماة المرحلة S.
ينقسم الصبغي طولياً خلال الانقسام الخيطي mitosis، مشكلاً كروماتيدتين يرتبطان معاً في منطقة القسيم المركزي (السنترومير). ثم ينفصل كروماتيد من كل شفع ليتجه إلى أحد قطبي الخلية، ويلي ذلك انقسام الخلية إلى خليتين تحتوي كل منهما على العدد الصبغي نفسه الذي احتوته الخلية الأم (2n).
أما في حالة الانقسام المنصف meiosisالمؤدي إلى تكوين الأعراس gametes، فإن الكروموزومات تتضاعف مرة واحدة، ولكن الخلية تنقسم مرتين متتاليتين، الثانية منهما خيطية، فتمتلك كل من الأعراس الأربعة الناتجة من هذين الانقسامين نصف العدد الصبغي الموجود في الخلايا الجسمية. ويعود العدد الصبغي إلى حالته الضعفانية عند حدوث عملية الإخصاب fertilization.
القسيمات الانتهائية (التيلوميرات) telomeres: وهي تتاليات من الدنا تغطي أطراف الصبغيات. و تتكون في معظم الكائنات من نسخ كثيرة من تتاليات قصيرة من الدنا، فمثلاً، يتكون التليومير في صبغي الإنسان من نحو مليوني نسخة من تتالٍ عشوائي TTAGGG (نحو 10000ـ 15000كيلوقاعدة kilobase). تلعب هذه القسيمات دوراً مهماً في ثبات الصبغيات وتمنع أطرافها من الالتصاق بعضها مع بعض، كما أنها تربط بروتينات معينة تحميها من أن تُهضم بفعل أنزيمات النوكليوزات الخارجيةexonucleases الموجودة في الخلية ذاتها. وتسمح القسيمات الانتهائية لتضاعف الدنا بأن يستمر حتى نهاية الصبغي، وقد يكون لها تأثير على نشاطات الجينات القريبة منها. وهنالك أدلة على أن فقدانها من الأطراف الصبغية مرتبط مع الشيخوخة وكذلك مع تكون الخلايا السرطانية.
التوابع microsatellites: هي قطع من الدنا تمتللك تتاليات عشوائية من القواعد، ويبين الجدول (3) بعضاً من أمثلتها:
يمكن إكثار هذه التتاليات مخبرياً باستخدام تفاعل البوليميراز التسلسلي PCR، وبالتالي يمكن تحديدها في موقع صبغي معين بسهولة، ويلاحظ منها وجود علامتين وراثيتين، إذ إن الفرد يرث إحدى التتاليات من أبيه والثانية من أمه.
تنتشر التوابع في جينومات حقيقيات النواة، وهي كثيرة التغير من فرد إلى آخر، ويسهل تحديدها وإكثارها بدءاً من كمية زهيدة بوساطة تفاعل البوليميراز التسلسلي، ولذلك تزايد استخدامها منذ منتصف ثمانينيات القرن العشرين في أمور التعرف الجنائي. ويكون ذلك بالربط بين المشتبه به وعينة من الدم أو الشعر أو السائل المنوي أخذت من موقع الجريمة، فيتم تحديد البصمة الوراثية [ر] للمشتبه به لمقارنتها مع تلك الناتجة من تحليل العينة الحيوية المتحصل عليها. أو تجرى لإثبات البنوة في حالة ادعاء أحد الأبوين بها وإنكار الآخر لها، أو في تحري بعض الأمراض كالسرطانات التي تسبب عادة تغيراً في أطوال التوابع في مراحلها المبكرة، وغير ذلك من استخدامات.
منطقة تكوين النوية nucleolus organizer region: هي منطقة في صبغي، أو عدة صبغيات، تحتوي عدداً من المورثات الناشطة في تكوين النويةnucleolus، وفي تركيب synthesis الحمض الريبي النووي الريبوزومي (rRNA) RNA ribosomal، وهذا النوع من الرنا مهم في عملية اصطناع البروتين. ويبلغ عدد هذه المناطق خمساً في الإنسان.
الصبغيات الصنعية: تعترض الباحثون في مجالات الهندسة الوراثية صعوبات التحكم الدقيق في أماكن إدماج مورثات منقولة إلى صبغيات معينة، فيكون ذلك الاندماج عشوائياً، وقد يؤثر ذلك تأثيراً سيئاً في الجينات الأساسية أو المنقولة، أو تكون له أضرار على الكائن نفسه، ولذلك يسعى العلماء لتكوين صبغيات صنعيةartificial chromosomes قادرة على تكرار ذاتها في كل انقسام خلوي، وكذلك على الانتقال من جيل إلى آخر عبر الأعراس. وبحيث تمتلك جميع المكونات اللازمة لسلامتها واستمراريتها، وخاصة منطقة التكاثر والتيلوميرات والقسيمات المركزية، وأن تكون قادرة على نقل أجزاء كبيرة من الدنا إلى الخلايا المرغوبة.
يمكن أن توفر الصبغيات الصنعية فوائد كبيرة، كأن تفسر بوضوح كيفية تضاعف الصبغيات بدقة، وطرائق انفصالها في أثناء الانقسام الخلوي وتوجهها إلى خلايا جديدة، كذلك يأمل الباحثون أن يتعرفوا تأثير البيئة المحيطة بالجينات في أنشطتها بعد إدخالها إلى الخلايا بوساطة هذه الصبغيات. ويمكن أن تستفيد المعالجة الجينية من الصبغيات الصنعية، إذ يتطلع الباحثون إلى التمكن من إدخال مورثات معينة بوساطتها إلى خلايا إنسان مريض فتساعد في شفائه.
وقد تمكن بعض الباحثين من تكوين صبغيات صنعية في الخميرة والفأر، وتحقق نجاح محدود في تكوين صبغي صنعي بشري، إلا أن بحوثهم لم تحقق النجاح المأمول حتى اليوم، ولم يتمكن أحد من تكوين صبغيات صنعية ثابتة في الخلايا المحضّنة إلى وقت طويل، ويؤمل تحقيق ذلك في المستقبل القريب.
أسامة عارف العوا
الصبغي (الكروموزوم) chromosome، جسيم مجهري خيطي الشكل كثير الالتفاف، تترتب الجينات (المورثات) genes على امتداده، وقد اشتقت كلمة كروموزوم من كلمتين يونانيتين هما Chromo (لون) وsoma(جسم)، لأن الصبغي يمكن تلوينه بأصبغة معينة.
يُعد العالم الألماني والتر فليمنغ(1843ـ1905) Walter Flemming مؤسس علم الوراثة الخلوية، أول من درس ووصف سلوك الصبغيات ضمن نواة الخلية في أثناء الانقسام الخلوي العادي (الخيطي أو الفتيلي)mitosis. ففي عام 1879 لاحظ فليمنغ أن بعض أصبغة الأنوية الخلوية أظهر فيها مادة خيطية الشكل. فاستخدم تلك الأصبغة في خلايا تم «قتلها» في مراحل مختلفة من الانقسام، ولاحظ سلسلة من التغيرات تحدث ضمن الأنوية، وأوضح أن تلك «الخيوط»، التي أسماها فلهيلم فون فولدير Wilhelm von Waldeyer «كرموزومات» (صبغيات)، قد قصرت أطوالها وانشطرت طولياً إلى أنصاف، توجه كل نصف منها إلى أحد قطبي الخلية. وأطلق فليمنغ على هذه العملية اسم الانقسام العادي (الخيطي أو الفتيلي) ووصفها عام 1882 في كتابه المهم «المادة الخلوية، النواة، والانقسام الخلوي» Zell-substanz, Kern und Zelltheilung ولم تُعرّف أهمية دراساته في مجالات الوراثة إلا بعد اكتشاف قوانين مندل[ر] بعد نحو عقدين من الزمن.
تطورت دراسات الانقسام الخلوي وسلوك الصبغيات منذ النصف الثاني من القرن التاسع عشر، وفي عام 1900، أعيد اكتشاف قوانين مندل من قبل كورينسCorrens وتشيرماك Tschermakودوفريس De Vries، بعد تجاهلها نحو 35سنة. وفي عام 1903، قدم ساتونW.S.Sutton التفسير الواضح الأول للعلاقة بين «العوامل» الوراثية التي اقترحها مندل (وأُسميت فيما بعد الجينات genes «أو المُوَرِّثات») وبين الصبغيات. وتتابعت أبحاث واكتشافات باهرة في القرن العشرين الذي يمكن تسميته قرن الثورة الوراثية، ولاشك أن أبرزها كان اكتشاف واطسون Watsonوكريك Crick عام 1953 التركيب الحلزوني المضاعف للحمض الريبي النووي المنقوص الأكسجين deoxyribonucleic acid (الدناDNA).
بنية الصبغي
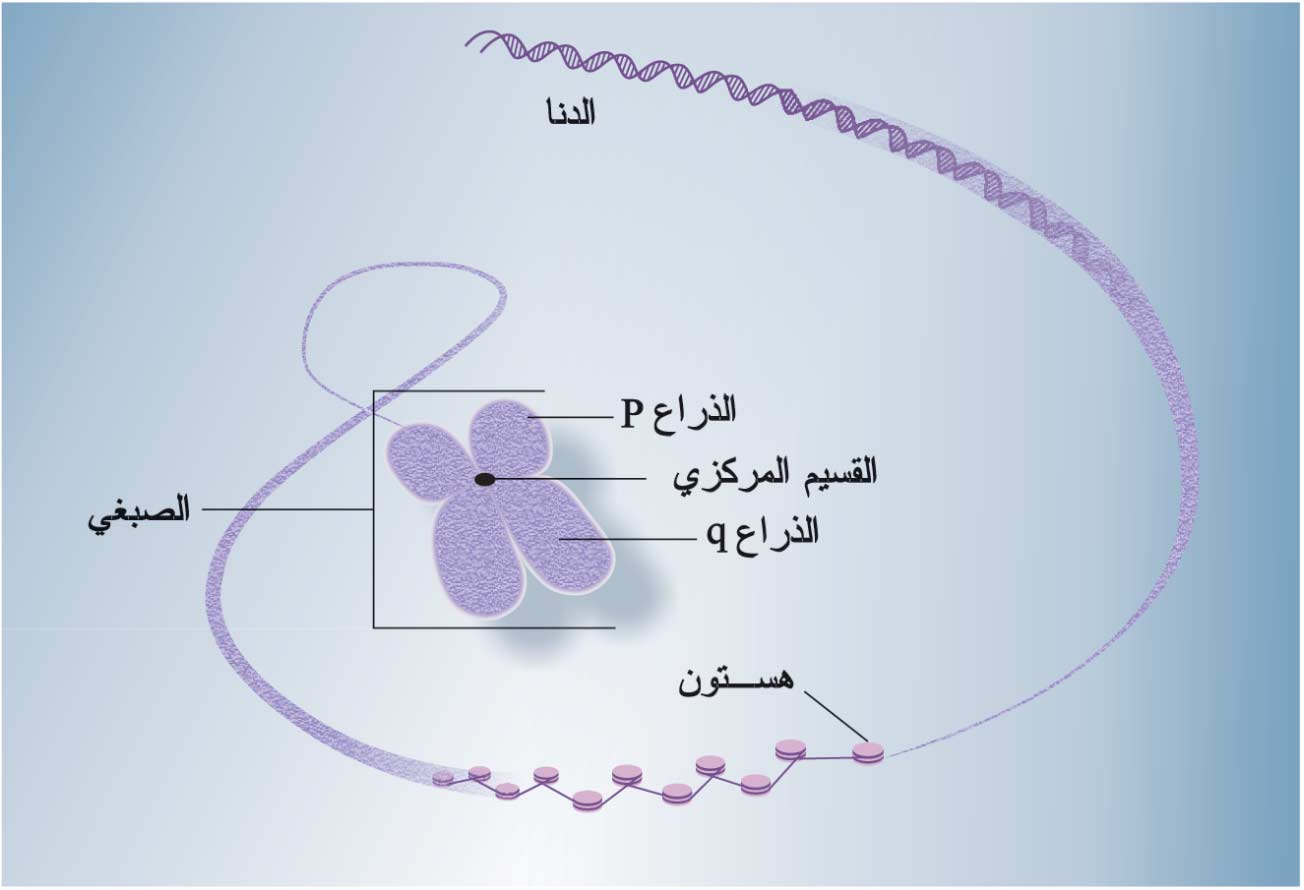 |
| الشكل (1) تركيب الصبغي |
الصبغيات جسيمات بالغة الدقة والالتفاف (الشكل 1)، تتألف من الحمض الريبي النووي المنقوص الأكسجين (الدناDNA)، ولو أمكن فَرْدُ دنا صبغيات خلية إنسانية واحدة ووصلت فيما بينها لبلغ طولها نحو المترين. وبهذه الالتفافات تتمكن النواة، التي لايتجاوز قطر الخلية التي تحويها نحو 6ميكرومتر، من احتواء دنا الصبغيات الستة والأربعين الخاصة بالإنسان، ويحقق ذلك عدة مستويات من الالتفاف coiling، بمساعدة بروتينات الكروماتين، مما يؤدي إلى إنقاص حجم الصبغي نحو 8آلاف مرة عما هو عليه في الدور البيني interphase. ويُراوح طول جزيء الدنا في الصبغي البشري بين نحو 50×10 6زوج من النيوكليوتيدات في أصغر صبغي (يبلغ طوله إذا فُرِد نحو 1.7سم) و نحو 250×10 6زوج منها في أطول صبغي (يبلغ طوله إذا فُرد نحو 8.5سم).
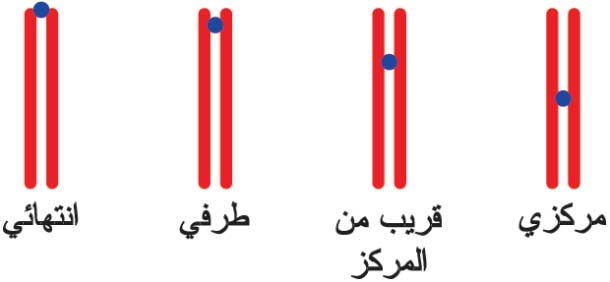 |
| الشكل (2) موقع القسيم المركزي على الصبغي |
 |
| الشكل (3) دور القسيمات المركزية في جذب الكروماتيدات على الخيوط المغزلية في أثناء الانقسام الخلوي |
تتكون البروتينات عند القسيم المركزي مشكلة نقاط ارتباط الكروماتيدات مع الخيوط المغزلية (الشكل 3) في أثناء الدور الثاني (الاستوائي) من الانقسام الخيطي، أو الصبغيات في الانقسام المنصف، لترحل في الدور الثالث نحو قطبي الخلية.
الدنا هو المادة الوراثية في الكائنات الحية، وتمتلك كل خلية في جسم الفرد من نوع معين الدنا ذاته (إلا في حال حدوث طفرات أو شذوذ صبغي). وتتركز غالبية الدنا ضمن أنوية الخلايا، بينما تحتوي المتقدرات (الميتوكوندريا) mitochondria على كميات قليلة منه. ويخزِّن الدنا التعليمات الوراثية بشكل مرمَّز coded من أربعة حروف يمثل كل منها اسم قاعدة هي: الأدينين adenine (A)والغوانين guanine (G) والسيتوزين cytosine (C) والثيمين thymine (T). ويتكون دنا الإنسان من نحو 3مليار قاعدة، أكثر من 99% منها متماثل في كل البشر. وتعمل تتاليات القواعد على تحديد البيانات التي ستستخدم لبناء الكائن الحي والمحافظة عليه. ويوضح الجدول (1) اختلاف أعداد القواعد في بعض الصبغيات.
|
||||||||||||||||||
تحتوي الصبغيات على الغالبية العظمى من الجينات، ويستثنى من ذلك العدد الضئيل منها في المتقدرات، والضروري لتكوين مركب ثالث فسفات الأدينوزين adenosine triphosphate (ATP) الغني بالطاقة، وفي الصانعات الخضر chloroplasts الضرورية لعملية التركيب الضوئي photosynthesis.
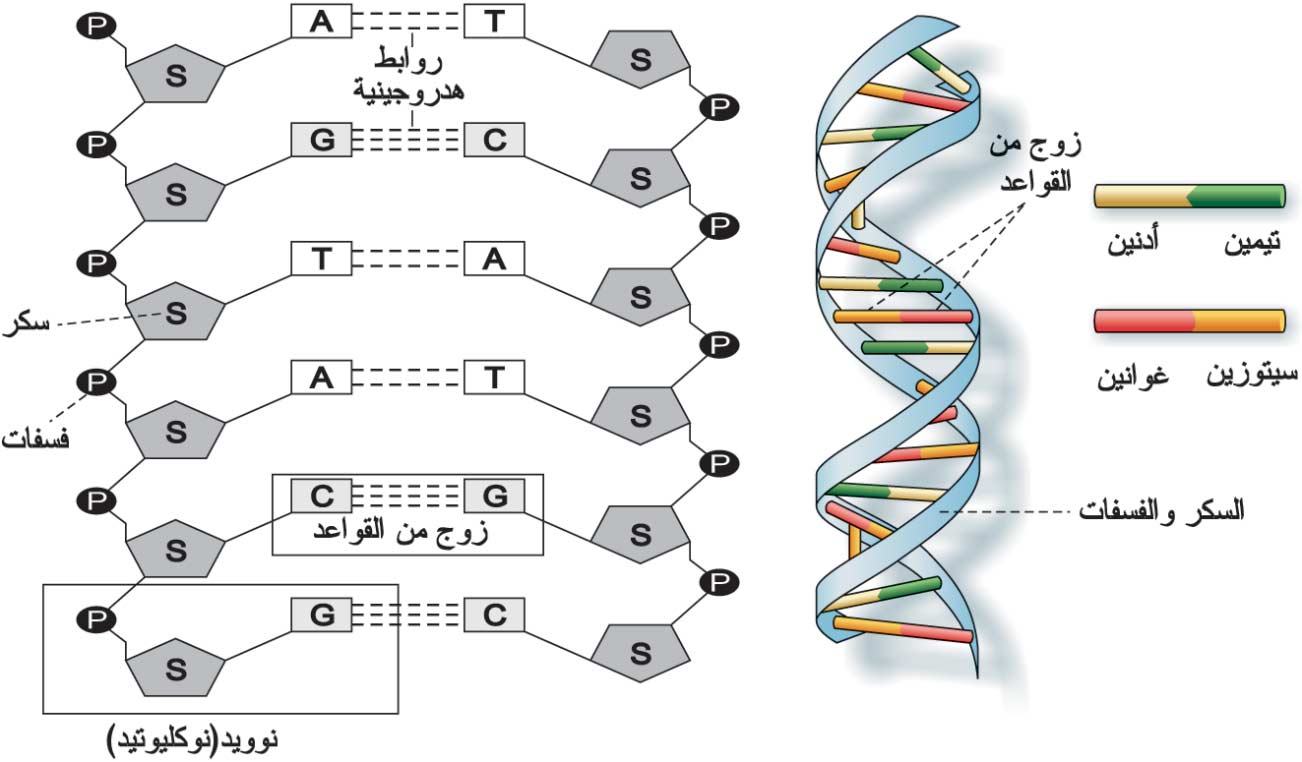 |
| الشكل (4) رسمان تخطيطيان للدنا |
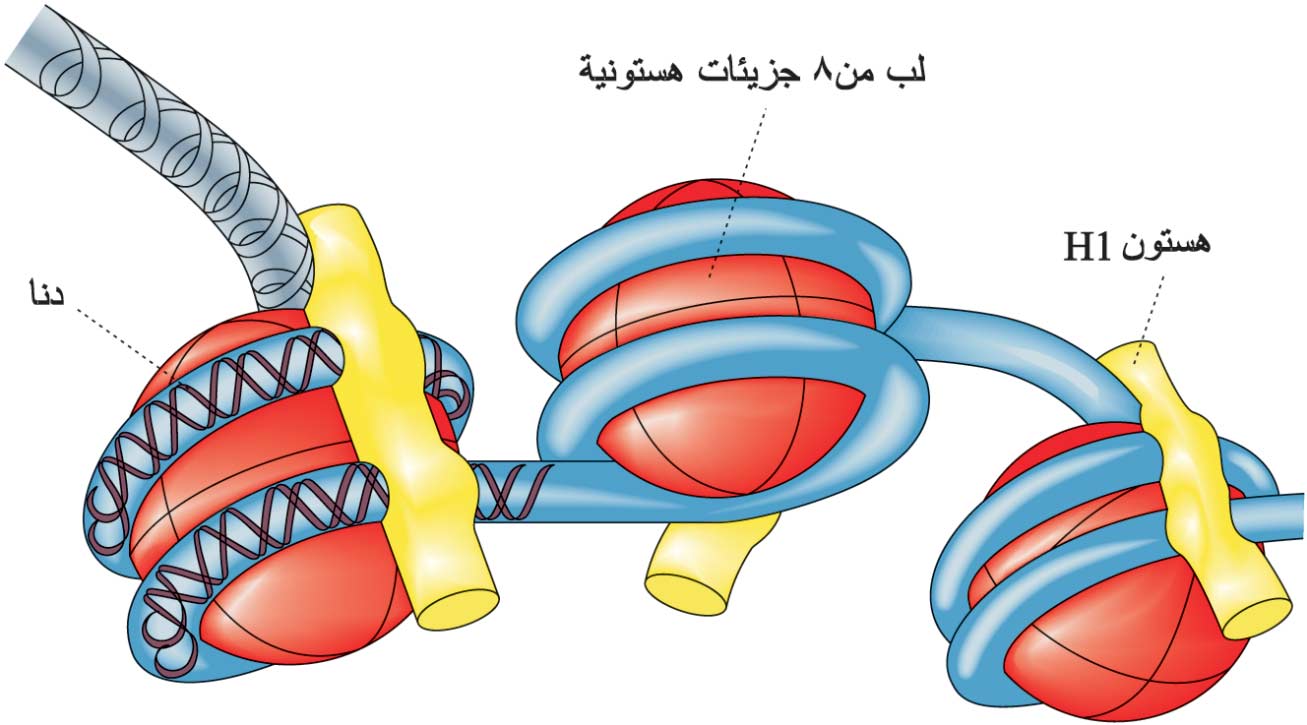 |
| الشكل (5) التفاف الدنا حول الهستون وتشكل النوكليوزومات |
 |
| الشكل (6) الصبغي في البكتيريا |
تقوم الهستونات بدور مهم في تكثيف الدنا ضمن الصبغيات، ويمكن باستخدام المجهر الإلكتروني مشاهدة حبات beadsقطر كل منها نحو 100أنغستروم مرتبة على صبغي سبق أن عومل بمنظفات detergentsمعينة، تدعى النوكليوزومات nucleosomes، تتكون من الدنا ونسختين من كل من الهستونات H2a, H2b, H3, H4، ويلتف نحو 200زوج من القواعد حولها مرتين، أما الهستون H1 فإنه يكون بين النوكليوزيدات على الدنا (الشكل 5)، فيحقق ذلك تكثيفاً أشد للدنا. ويبلغ قصر الصبغي حده الأقصى في الطورين الثاني metaphase والثالثanaphase من الانقسام الخلوي.
يضاف إلى ذلك عدد قليل من النسخ من عدة أنواع من البروتينات غير الهستونية، معظمها عوامل انتساخ transcription factorsتنظم أجزاء الدنا التي سوف يتم انتساخها إلى حمض ريبي نووي ribonucleic acid (رناRNA)، وتعمل هذه البروتينات على ضغط النيوكليوسومات أكثر بشكل لفّات مدمجة.
أما في الكائنات البدائية النواةprokaryotes، كالبكتريا، فإن الصبغي يتألف من دنا حلقي غير محاط بغلاف نووي (الشكل 6).
يطلق على المعقد المكوَّن من الحموض النووية (DNA وRNA) والبروتينات اسم الكروماتين chromatin. ويقسم إلى نوعين:
1ـ الكروماتين السوي euchromatin: وهو جزء الصبغي الذي لايقبل الصبغ أو يقبله قليلاً، ويعتقد أنه يحوي الجينات الفعالة، ويشاهد في الخلايا النشيطة. وإن وجود هذا الكروماتين مهم لحاجة المناطق التي ستُستنسخ أو تتضاعف إلى فك الالتفاف قبل أن يمكن قراءة الشفرة الوراثية.
2ـ الكروماتين المتغاير heterochromatin: وهو كروماتين مكثف يقبل الصبغ بشدة، ويعتقد أن معظمه خامل وراثياً. يظل هذا الكروماتين ملتفاً بشدة خلال الدورة الخلوية، ويُشاهد في بعض الأحيان مجاوراً للغلاف النووي، ولكنه يكون آنذاك مقطعاً بمناطق فاتحة عند مسام pores الغلاف المذكور، مما يُسهل عمليات التبادل بين النواة والهيولى (السيتوبلازم).
الأعداد الصبغية
|
||||||||||||||||||||||||||||||||
ومن جهة أخرى، فإن الصبغيات تصنَّف في مجموعتين:
ـ الصبغيات الجسمية (A)autosomes، التي لاتختلف بين الذكور والإناث.
ـ صبغيا الجنس sex chromosomes، وهما متماثلان في إناث الثدييات، يرمز لكل منهما بـ X، ومختلفان في ذكورها، حيث يكون أحدهما X والثاني أصغر حجماً ويرمز له بـ Y، وعلى هذا تكون الصيغة الصبغية للرجل 44A+XY وللمرأة 44A+X.
تشترك جميع الكائنات الحقيقية النواة التي تمت دراستها بكون صبغياتها ضعفانية العدد، لاتقل عن اثنين، وبامتلاكها دنا خيطي الشكل. والاختلاف الرئيس بينها هو في عدد الصبغيات، ويبدو أن هذا العدد ليس مرتبطاً بالصفات الحيوية للنوع، فمثلاً، يوجدفي الخميرة 16صبغياً، أي أربعة أضعاف ماتمتلكه ذبابة الخل[ر]. كما أن عدد الصبغيات ليس مرهوناً بحجم الجينوم، فمثلاً يوجد في بعض أنواع السلمندل salamanderجينوماً يزيد على ما يحوي في جينوم الإنسان بنحو 30مرة، ولكن عدد صبغياتها نصف عدد صبغيات الإنسان. ومع أهمية هذه الملاحظات، فإنها لاتدل إلا على عدم التجانس في عمليات التطور التي أدت إلى تحديد الأعداد الصبغية والجينومات في الأنواع المختلفة.
تعيين موقع الجين على الصبغي
 |
| الشكل (7) مكان الجين CFTR في الموقع s7q31.2 |
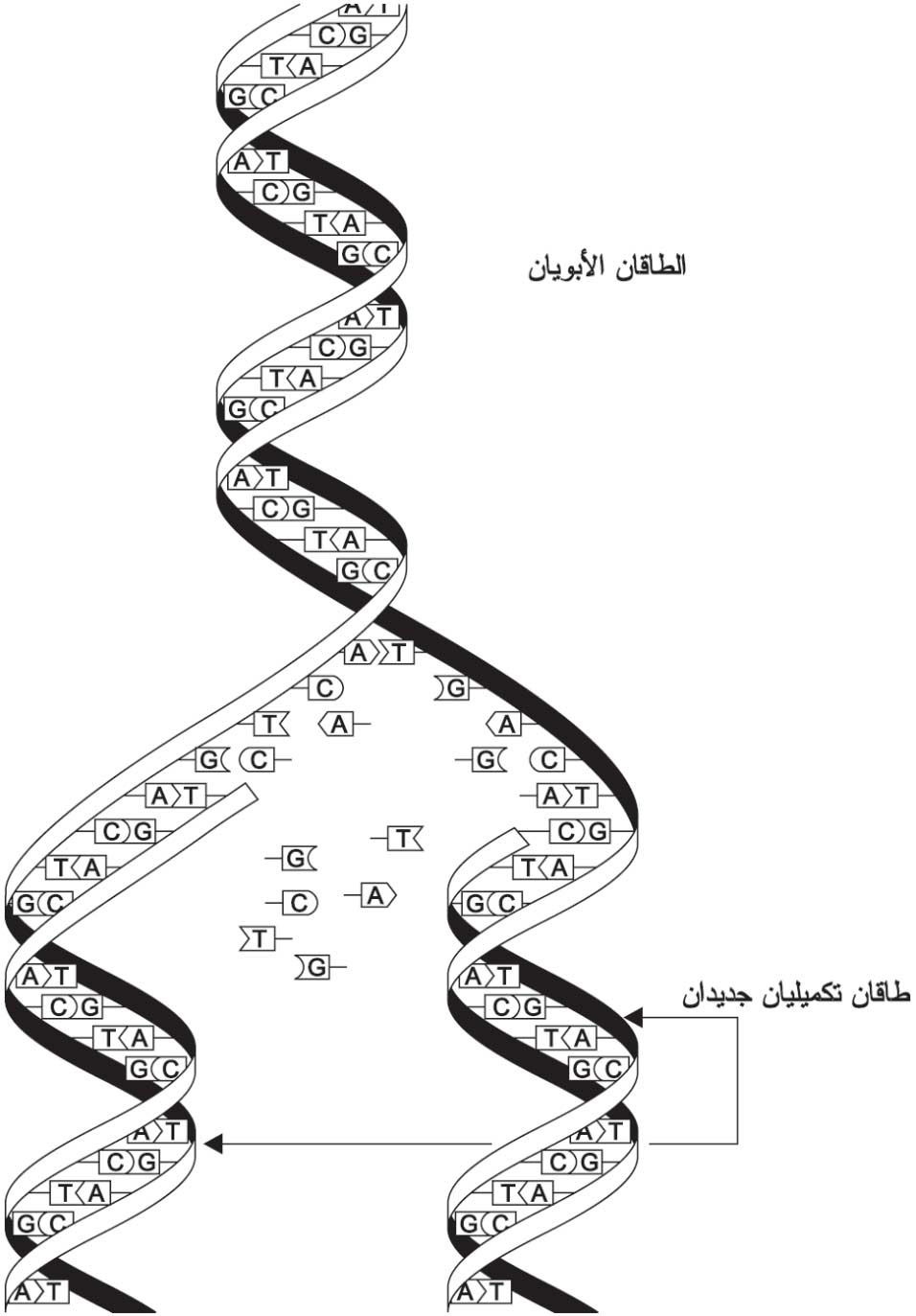 |
| الشكل (8) انشطار الدنا |
لكل جين موقع خاص به على صبغي معين، ويمكن تحديده بكتابته كموقع محدد:s17q12، أوبين حدين (مدى) إذا لم يكن الموقع محدداً بدقة: s17q12-q21.
توفر الأعداد والحروف بهذه الطريقة «عنواناً» لموقع كل جين على صبغي. ويتألف هذا العنوان من الآتي:
ـ رقم الصبغي الذي يوجد الجين فيه، وهو 17 في المثالين السابقين. وتمثل الصبغيات الجسمية 1ـ22 بأرقامها، أما الصبغيان الجنسيان فيشار إليهما بـ X أو Y.
ـ يقسم الصبغي إلى ذراعين، يدعى القصير منهما p والطويل q. ورمز الذراع هو الجزء الثاني من عنوان الجين، إذ يلي رقم الصبغي مباشرة. فمثلاً 7q هي الذراع الطويل من الصبغي السابع، بينما Xp هي الذراع القصير من الصبغي X.
ـ موقع الجين على الذراع القصير أو الطويل. ويزداد هذا الرقم مع ازدياد بعد الجين عن القسيم المركزي. وقد بُنيَ الموقع الدقيق للجين على نظام العصيبات bandsالداكنة والفاتحة التي تميز الصبغي وتظهر بعد الصبغ (الشكل 7). ويكون ذلك باستخدام رقمين: أولهما هو رمز المنطقةregion، وثانيهما رمز العصيبة، وقد يُتبعان بفاصلة عشرية يليها رقم أو أكثر (تمثل أجزاء العصيبات sub-bands ضمن منطقة داكنة أو فاتحة).
ـ وقد يضاف أحياناً أحد المقطعين terأو cen للإشارة إلى أن المورثة قريبة جداً من القسيم المركزي، مثلاً: 16pcen، أو أنه قريب جداً من نهاية الذراع، مثلاً: 14 qter، أو يستخدم المقطع tel للإشارة إلى أن الجين موجود في التيلومير في نهاية الذراع.
تضاعف الدنا DNA Replication
الانقسامات الخلوية عملية معقدة ومهمة تمكن الكائن الحي من النمو في المراحل الأولى من عمره، ومن تكوين خلايا تعوِّض الخلايا التالفة أو المعمرة. وتسمح الصبغيات للدنا بأن يعيد إنتاج ذاته (الشكل 8)، وبالتالي فإن كلاً من الخليتين البنتين الناتجتين من الانقسام الخلوي تحتوي على جميع الجينات الموجودة في الخلية الأم.
للصبغيات قدرة كبيرة على تغيير أشكالها وأحجامها إبان الدورة الخلوية. ففي الطور البيني interphase من هذه الدورة، وهي الأطول، فإن دنا الجينات النشيطة يكون معرضاً لتأثير الأنزيمات الضرورية لاصطناع الحمض الريبي النووي (الرنا RNA)، وكذلك في مرحلة تضاعف الدنا والتي تشمل جزيء الدنا بكامله، والمسماة المرحلة S.
ينقسم الصبغي طولياً خلال الانقسام الخيطي mitosis، مشكلاً كروماتيدتين يرتبطان معاً في منطقة القسيم المركزي (السنترومير). ثم ينفصل كروماتيد من كل شفع ليتجه إلى أحد قطبي الخلية، ويلي ذلك انقسام الخلية إلى خليتين تحتوي كل منهما على العدد الصبغي نفسه الذي احتوته الخلية الأم (2n).
أما في حالة الانقسام المنصف meiosisالمؤدي إلى تكوين الأعراس gametes، فإن الكروموزومات تتضاعف مرة واحدة، ولكن الخلية تنقسم مرتين متتاليتين، الثانية منهما خيطية، فتمتلك كل من الأعراس الأربعة الناتجة من هذين الانقسامين نصف العدد الصبغي الموجود في الخلايا الجسمية. ويعود العدد الصبغي إلى حالته الضعفانية عند حدوث عملية الإخصاب fertilization.
القسيمات الانتهائية (التيلوميرات) telomeres: وهي تتاليات من الدنا تغطي أطراف الصبغيات. و تتكون في معظم الكائنات من نسخ كثيرة من تتاليات قصيرة من الدنا، فمثلاً، يتكون التليومير في صبغي الإنسان من نحو مليوني نسخة من تتالٍ عشوائي TTAGGG (نحو 10000ـ 15000كيلوقاعدة kilobase). تلعب هذه القسيمات دوراً مهماً في ثبات الصبغيات وتمنع أطرافها من الالتصاق بعضها مع بعض، كما أنها تربط بروتينات معينة تحميها من أن تُهضم بفعل أنزيمات النوكليوزات الخارجيةexonucleases الموجودة في الخلية ذاتها. وتسمح القسيمات الانتهائية لتضاعف الدنا بأن يستمر حتى نهاية الصبغي، وقد يكون لها تأثير على نشاطات الجينات القريبة منها. وهنالك أدلة على أن فقدانها من الأطراف الصبغية مرتبط مع الشيخوخة وكذلك مع تكون الخلايا السرطانية.
التوابع microsatellites: هي قطع من الدنا تمتللك تتاليات عشوائية من القواعد، ويبين الجدول (3) بعضاً من أمثلتها:
|
||||||||||||
تنتشر التوابع في جينومات حقيقيات النواة، وهي كثيرة التغير من فرد إلى آخر، ويسهل تحديدها وإكثارها بدءاً من كمية زهيدة بوساطة تفاعل البوليميراز التسلسلي، ولذلك تزايد استخدامها منذ منتصف ثمانينيات القرن العشرين في أمور التعرف الجنائي. ويكون ذلك بالربط بين المشتبه به وعينة من الدم أو الشعر أو السائل المنوي أخذت من موقع الجريمة، فيتم تحديد البصمة الوراثية [ر] للمشتبه به لمقارنتها مع تلك الناتجة من تحليل العينة الحيوية المتحصل عليها. أو تجرى لإثبات البنوة في حالة ادعاء أحد الأبوين بها وإنكار الآخر لها، أو في تحري بعض الأمراض كالسرطانات التي تسبب عادة تغيراً في أطوال التوابع في مراحلها المبكرة، وغير ذلك من استخدامات.
منطقة تكوين النوية nucleolus organizer region: هي منطقة في صبغي، أو عدة صبغيات، تحتوي عدداً من المورثات الناشطة في تكوين النويةnucleolus، وفي تركيب synthesis الحمض الريبي النووي الريبوزومي (rRNA) RNA ribosomal، وهذا النوع من الرنا مهم في عملية اصطناع البروتين. ويبلغ عدد هذه المناطق خمساً في الإنسان.
الصبغيات الصنعية: تعترض الباحثون في مجالات الهندسة الوراثية صعوبات التحكم الدقيق في أماكن إدماج مورثات منقولة إلى صبغيات معينة، فيكون ذلك الاندماج عشوائياً، وقد يؤثر ذلك تأثيراً سيئاً في الجينات الأساسية أو المنقولة، أو تكون له أضرار على الكائن نفسه، ولذلك يسعى العلماء لتكوين صبغيات صنعيةartificial chromosomes قادرة على تكرار ذاتها في كل انقسام خلوي، وكذلك على الانتقال من جيل إلى آخر عبر الأعراس. وبحيث تمتلك جميع المكونات اللازمة لسلامتها واستمراريتها، وخاصة منطقة التكاثر والتيلوميرات والقسيمات المركزية، وأن تكون قادرة على نقل أجزاء كبيرة من الدنا إلى الخلايا المرغوبة.
يمكن أن توفر الصبغيات الصنعية فوائد كبيرة، كأن تفسر بوضوح كيفية تضاعف الصبغيات بدقة، وطرائق انفصالها في أثناء الانقسام الخلوي وتوجهها إلى خلايا جديدة، كذلك يأمل الباحثون أن يتعرفوا تأثير البيئة المحيطة بالجينات في أنشطتها بعد إدخالها إلى الخلايا بوساطة هذه الصبغيات. ويمكن أن تستفيد المعالجة الجينية من الصبغيات الصنعية، إذ يتطلع الباحثون إلى التمكن من إدخال مورثات معينة بوساطتها إلى خلايا إنسان مريض فتساعد في شفائه.
وقد تمكن بعض الباحثين من تكوين صبغيات صنعية في الخميرة والفأر، وتحقق نجاح محدود في تكوين صبغي صنعي بشري، إلا أن بحوثهم لم تحقق النجاح المأمول حتى اليوم، ولم يتمكن أحد من تكوين صبغيات صنعية ثابتة في الخلايا المحضّنة إلى وقت طويل، ويؤمل تحقيق ذلك في المستقبل القريب.
أسامة عارف العوا
