اكتشف الباحثون طريقة لإعادة برمجة خلايا الجلد مباشرةً إلى خلايا عصوية مستقبلة للضوء تُستخدم في الرؤية، مكنت العصي المصنَّعة مخبريًا الفئران العمياء من إبصار النور بعد زرعها في عيونها، وقد نُشر العمل الممول أصلًا من المعهد الوطني للعيون -وهو قسم من المعاهد الوطنية للصحة- في 15 أبريل.
استبدل الباحثون المستقبلات الضوئية التالفة في النماذج الحيوانية -حتى اللحظة- عن طريق تشكيل خلايا جذعية من خلايا الجلد أو الدم وبرمجتها لتصبح مستقبلات ضوئية ثم زرعها في القسم الخلفي للعين، أظهر العلماء في الدراسة الجديدة إمكانية تجاوز مرحلة توسّط الخلايا الجذعية وإعادة برمجة خلايا الجلد مباشرة إلى مستقبلات ضوئية تُزرع في شبكية العين.
يقول الدكتور أناند سواروب كبير الباحثين في مختبر البيولوجيا العصبية والتنكس العصبي وعلاجه في المعهد الوطني للعيون، والذي ميّز العصي المُستقبلة للضوء المُعاد برمجتها عن طريق تحليل التعبير الجيني: «هذه أول دراسة تُظهر إمكانية إنتاج خلايا تشبه الشبكية من خلال إعادة البرمجة الكيميائية المباشرة ما يمنحنا استراتيجية جديدة وسريعة لتطوير علاجات التنكس البقعي المرتبط بالعمر واضطرابات الشبكية الأخرى الناجمة عن خسارة المستقبلات الضوئية».
قال أيضًا: «ستكون القدرة على التطوير السريع لأشكال المرض وبالتالي القدرة على دراسة آلياته إحدى الفوائد الفورية للاستراتيجية الجديدة، والتي ستساعدنا أيضًا على تصميم أساليب أفضل لاستبدال الخلايا».
درس العلماء الخلايا الجذعية المُحفّزة متعددة القدرات باهتمام شديد في العقد الماضي، تُطوَّر هذه الخلايا في مختبر من الخلايا الناضجة -بدلًا من أنسجة الجنين- ويمكن استخدامها لصنع أي نوع تقريبًا من الخلايا أو الأنسجة البديلة، لكن قد تستغرق بروتوكولات إعادة برمجة هذه الخلايا ستة أشهر قبل أن تصبح جاهزة للزرع، بالمقابل حوّلت إعادة البرمجة المباشرة المذكورة في الدراسة الحالية خلايا الجلد إلى خلايا عصوية مستقبلة للضوء وظيفية جاهزة للزراعة خلال 10 أيام فقط، وقد استخدم الباحثون لإثبات فعاليتها في عيون الفئران خلايا الجلد المُستمدة من الفئران والبشر.
قال الطبيب ساي شافالا كبير الباحثين في الدراسة والرئيس التنفيذي ورئيس شركة (CIRC) لعلم المداواة ورئيس مركز تصنيع شبكية العين: «تحوّل تقنيتنا خلايا الجلد مباشرة إلى مستقبلات ضوئية دون الحاجة إلى خلايا جذعية بينها»، شافالا هو أيضًا مدير خدمات العناية بشبكية العين في مراكز العناية بالعين في تكساس وأستاذ جراحة في جامعة تكساس المسيحية في كلية الطب في مركز العلوم الصحية لجامعة شمال تكساس في فورت وورث.
تتضمن إعادة البرمجة المباشرة غمر خلايا الجلد في مزيج من خمسة مركبات جزيئية صغيرة تقوم بدور الوسيط الكيميائي في مسارات الجزيئات المرتبطة بمصير خلايا العصي المستقبلة للضوء للحصول على خلايا عصوية مستقبلة للضوء تحاكي العصي الأصلية في المظهر والوظيفة.
أوضح الباحثون من خلال تنميط التعبير الجيني تشابه الجينات التي تعبّر عنها الخلايا الجديدة مع الجينات التي عبّرت عنها خلايا العصي المستقبلة للضوء الحقيقية وفي الوقت نفسه تعطيل التنظيم الجيني المسؤول عن وظيفة خلايا الجلد.
زرع الباحثون الخلايا في عيون الفئران المصابة بتنكّس الشبكية ثم اختبروا ردود أفعال حدقاتها باعتباره مقياسًا لوظيفة المستقبلات الضوئية بعد الزرع، إذ يعتمد انقباض الحدقة في ظروف الإضاءة المنخفضة على وظيفة المستقبلات الضوئية، أظهرت ستة حيوانات من أصل 14 أي 43٪ خلال أشهر من الزرع انقباضًا قويًا للحدقة في ظروف الإضاءة المنخفضة مقارنة بالمجموعة التي لم تتلقَ علاجًا.
علاوة على ذلك كانت الفئران المعالجة التي أظهرت انقباضًا في الحدقة أكثر سعيًا إلى التواجد في الأماكن المظلمة وقضاء الوقت فيها مقارنةً بالفئران غير المعالجة أو المعالجة دون استجابة الحدقة، يتطلب سلوك تفضيل الأماكن المظلمة القدرة على الرؤية ويعكس الميل الطبيعي للفأر للبحث عن مواقع مظلمة آمنة بدلاً من المواقع المنارة.
قال الدكتور بيراج ماهاتو المؤلف الأول للدراسة وعالم أبحاث في مركز العلوم الصحية لجامعة شمال تكساس: «حتّى الفئران المصابة بتنكّس شبكية شديد ومتقدم -ذات الفرصة الضئيلة ببقاء مستقبلات ضوئية حية- استجابت لعملية الزرع، ما يوضّح دور المستقبلات الضوئية المصنّعة مخبريًّا في التحسينات المُلاحظة أكثر من الدور المساعد للمستقبلات الضوئية السليمة المتواجدة مسبقًا في العين».
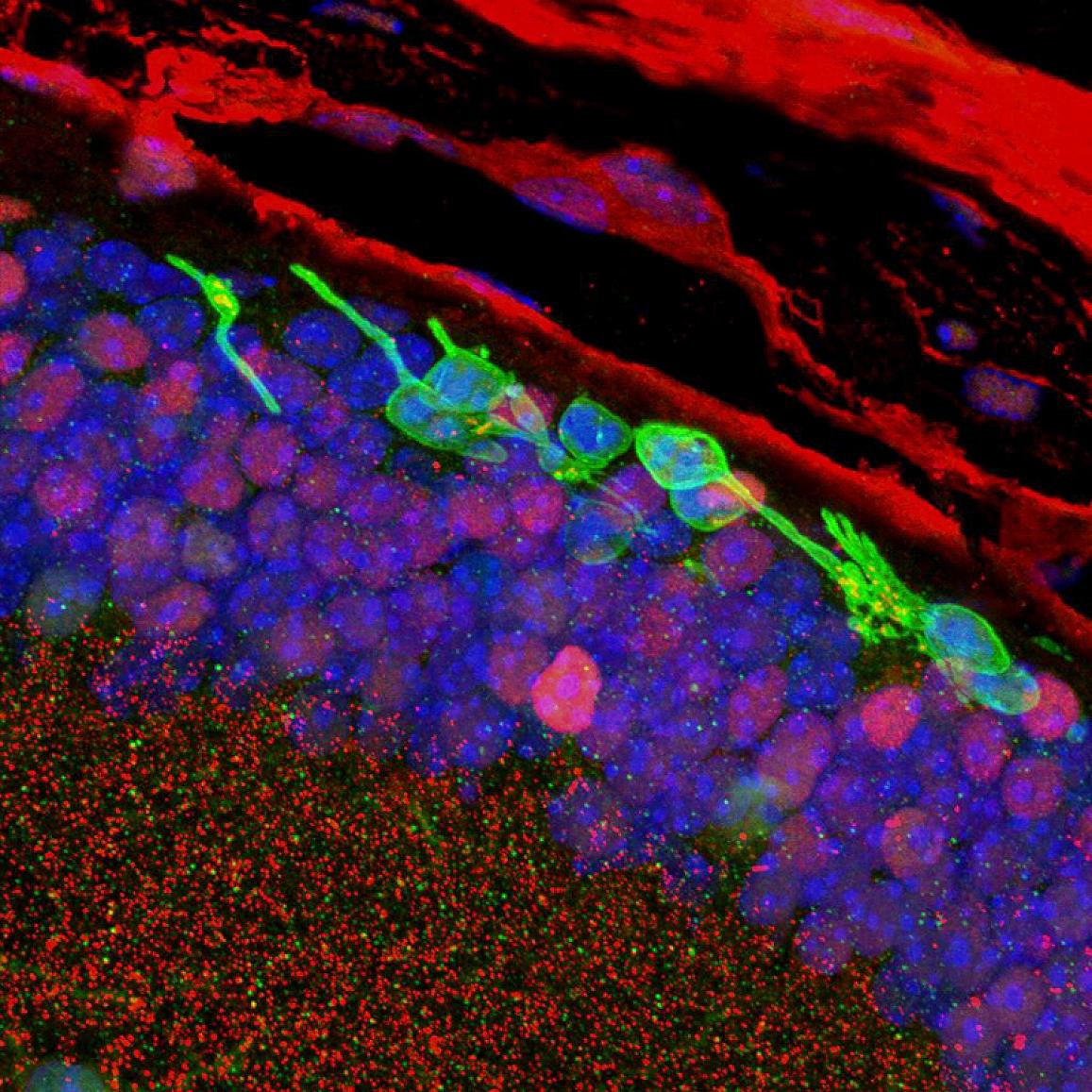
أكدت دراسات التألق المناعي بقاء المستقبلات الضوئية المصنّعة مخبريًا واتصالاتها المشبكية بالخلايا العصبية في الشبكية الداخلية بعد ثلاثة أشهر من الزرع، و لا زلنا نحتاج المزيد من البحث لتحسين البروتوكول بهدف زيادة عدد المستقبلات الضوئية الوظيفية المزروعة.
قال سواروب: «سيساعد نجاح الباحثين في معرفة كيفية توسيط إعادة البرمجة المباشرة على المستوى الخلوي على تطبيق التقنية على أنواع كثيرة من الخلايا الأخرى أيضًا لا خلايا شبكية العين فقط».
قال الدكتور كابيل بهارتي كبير الباحثين ورئيس قسم دراسة زرع الخلايا العينية والجذعية في المعهد الوطني للعيون: «قد يختصر تحسين كفاءة هذا التحويل المباشر-إذا كان ممكنًا- الكثير من الوقت الذي يحتاجه تطوير منتج علاجي مُحتمل للخلايا أو لنموذج المرض».
يخطط شافالا وزملاؤه لإجراء تجربة سريرية تختبر العلاج على البشر المصابين بأمراض الشبكية التنكسية مثل التهاب الشبكية الصباغي
استبدل الباحثون المستقبلات الضوئية التالفة في النماذج الحيوانية -حتى اللحظة- عن طريق تشكيل خلايا جذعية من خلايا الجلد أو الدم وبرمجتها لتصبح مستقبلات ضوئية ثم زرعها في القسم الخلفي للعين، أظهر العلماء في الدراسة الجديدة إمكانية تجاوز مرحلة توسّط الخلايا الجذعية وإعادة برمجة خلايا الجلد مباشرة إلى مستقبلات ضوئية تُزرع في شبكية العين.
يقول الدكتور أناند سواروب كبير الباحثين في مختبر البيولوجيا العصبية والتنكس العصبي وعلاجه في المعهد الوطني للعيون، والذي ميّز العصي المُستقبلة للضوء المُعاد برمجتها عن طريق تحليل التعبير الجيني: «هذه أول دراسة تُظهر إمكانية إنتاج خلايا تشبه الشبكية من خلال إعادة البرمجة الكيميائية المباشرة ما يمنحنا استراتيجية جديدة وسريعة لتطوير علاجات التنكس البقعي المرتبط بالعمر واضطرابات الشبكية الأخرى الناجمة عن خسارة المستقبلات الضوئية».
قال أيضًا: «ستكون القدرة على التطوير السريع لأشكال المرض وبالتالي القدرة على دراسة آلياته إحدى الفوائد الفورية للاستراتيجية الجديدة، والتي ستساعدنا أيضًا على تصميم أساليب أفضل لاستبدال الخلايا».

درس العلماء الخلايا الجذعية المُحفّزة متعددة القدرات باهتمام شديد في العقد الماضي، تُطوَّر هذه الخلايا في مختبر من الخلايا الناضجة -بدلًا من أنسجة الجنين- ويمكن استخدامها لصنع أي نوع تقريبًا من الخلايا أو الأنسجة البديلة، لكن قد تستغرق بروتوكولات إعادة برمجة هذه الخلايا ستة أشهر قبل أن تصبح جاهزة للزرع، بالمقابل حوّلت إعادة البرمجة المباشرة المذكورة في الدراسة الحالية خلايا الجلد إلى خلايا عصوية مستقبلة للضوء وظيفية جاهزة للزراعة خلال 10 أيام فقط، وقد استخدم الباحثون لإثبات فعاليتها في عيون الفئران خلايا الجلد المُستمدة من الفئران والبشر.
قال الطبيب ساي شافالا كبير الباحثين في الدراسة والرئيس التنفيذي ورئيس شركة (CIRC) لعلم المداواة ورئيس مركز تصنيع شبكية العين: «تحوّل تقنيتنا خلايا الجلد مباشرة إلى مستقبلات ضوئية دون الحاجة إلى خلايا جذعية بينها»، شافالا هو أيضًا مدير خدمات العناية بشبكية العين في مراكز العناية بالعين في تكساس وأستاذ جراحة في جامعة تكساس المسيحية في كلية الطب في مركز العلوم الصحية لجامعة شمال تكساس في فورت وورث.
تتضمن إعادة البرمجة المباشرة غمر خلايا الجلد في مزيج من خمسة مركبات جزيئية صغيرة تقوم بدور الوسيط الكيميائي في مسارات الجزيئات المرتبطة بمصير خلايا العصي المستقبلة للضوء للحصول على خلايا عصوية مستقبلة للضوء تحاكي العصي الأصلية في المظهر والوظيفة.
أوضح الباحثون من خلال تنميط التعبير الجيني تشابه الجينات التي تعبّر عنها الخلايا الجديدة مع الجينات التي عبّرت عنها خلايا العصي المستقبلة للضوء الحقيقية وفي الوقت نفسه تعطيل التنظيم الجيني المسؤول عن وظيفة خلايا الجلد.
زرع الباحثون الخلايا في عيون الفئران المصابة بتنكّس الشبكية ثم اختبروا ردود أفعال حدقاتها باعتباره مقياسًا لوظيفة المستقبلات الضوئية بعد الزرع، إذ يعتمد انقباض الحدقة في ظروف الإضاءة المنخفضة على وظيفة المستقبلات الضوئية، أظهرت ستة حيوانات من أصل 14 أي 43٪ خلال أشهر من الزرع انقباضًا قويًا للحدقة في ظروف الإضاءة المنخفضة مقارنة بالمجموعة التي لم تتلقَ علاجًا.
علاوة على ذلك كانت الفئران المعالجة التي أظهرت انقباضًا في الحدقة أكثر سعيًا إلى التواجد في الأماكن المظلمة وقضاء الوقت فيها مقارنةً بالفئران غير المعالجة أو المعالجة دون استجابة الحدقة، يتطلب سلوك تفضيل الأماكن المظلمة القدرة على الرؤية ويعكس الميل الطبيعي للفأر للبحث عن مواقع مظلمة آمنة بدلاً من المواقع المنارة.
قال الدكتور بيراج ماهاتو المؤلف الأول للدراسة وعالم أبحاث في مركز العلوم الصحية لجامعة شمال تكساس: «حتّى الفئران المصابة بتنكّس شبكية شديد ومتقدم -ذات الفرصة الضئيلة ببقاء مستقبلات ضوئية حية- استجابت لعملية الزرع، ما يوضّح دور المستقبلات الضوئية المصنّعة مخبريًّا في التحسينات المُلاحظة أكثر من الدور المساعد للمستقبلات الضوئية السليمة المتواجدة مسبقًا في العين».
أكدت دراسات التألق المناعي بقاء المستقبلات الضوئية المصنّعة مخبريًا واتصالاتها المشبكية بالخلايا العصبية في الشبكية الداخلية بعد ثلاثة أشهر من الزرع، و لا زلنا نحتاج المزيد من البحث لتحسين البروتوكول بهدف زيادة عدد المستقبلات الضوئية الوظيفية المزروعة.
قال سواروب: «سيساعد نجاح الباحثين في معرفة كيفية توسيط إعادة البرمجة المباشرة على المستوى الخلوي على تطبيق التقنية على أنواع كثيرة من الخلايا الأخرى أيضًا لا خلايا شبكية العين فقط».
قال الدكتور كابيل بهارتي كبير الباحثين ورئيس قسم دراسة زرع الخلايا العينية والجذعية في المعهد الوطني للعيون: «قد يختصر تحسين كفاءة هذا التحويل المباشر-إذا كان ممكنًا- الكثير من الوقت الذي يحتاجه تطوير منتج علاجي مُحتمل للخلايا أو لنموذج المرض».
يخطط شافالا وزملاؤه لإجراء تجربة سريرية تختبر العلاج على البشر المصابين بأمراض الشبكية التنكسية مثل التهاب الشبكية الصباغي
