الذرات هي الوحدات الأساسية للمادة والبنية المحدِدة للعناصر. ومصطلح (ذرة) يأتي من الكلمة اليونانية “Indivisible” وتعني «غير قابلة للتجزئة»، لأن اليونانيين آنذاك كانوا يعتقدون بأن الذرة هي أصغر الأشياء في الكون ولا يمكن تجزئتها. لكن نحن الآن نعرف أن الذرات تتكون من ثلاثة أنواع من الجسيمات (مكونات الذرة): البروتونات ، النيوترونات ، و الإلكترونات ، ونعلم أنها هي الأخرى مكونة من جزيئات أصغر حجمًا مثل الكواركات.
تشكلت الذرات بعد الانفجار الكبير أي قبل 13.7 مليار سنة. وعندما بدأ الكون الحار والكثيف جدًا بالتوسع أصبح أكثر برودة، وعندها سمحت الظروف بتكون الكواركات والإلكترونات. تجمعت الكواركات معًا لتشكيل البروتونات والنيوترونات، ودُمجت هذه الجسيمات في النواة. حدث هذا كله خلال الدقائق القليلة الأولى من نشأة الكون، وفقًا لـ”CERN”.

استغرق الكون 380,000 سنة حتى يبرد بدرجةٍ كافية لإبطاء الإلكترونات حتى تتمكن الأنوية من التقاطها لتشكيل أولى الذرات. وكانت أول الذرات هي الهيدروجين والهيليوم، اللذان لا يزالان أكثر العناصر وفرةً في الكون. ثم بدأت الجاذبية تسيطرعلى سُحب الغاز لتُشكل النجوم التي قامت بدورها بتشكيل ذرات أثقل (ولا تزال هذه العملية مستمرة إلى اليوم) وعند موت النجم ينفجر في حدث هائل يدعى بـ(المستعر الأعظم – Supernova)، ناشرًا محتواه الثمين في أرجاء الكون.
الجزيئات الذرية (مكونات الذرة)
البروتونات والنيوترونات أثقل من الإلكترونات وتستقر في النواة التي هي مركز الذرة. الإلكترونات خفيفة الوزن للغاية وتوجد في سحابة تدور حول النواة. يبلغ نصف قطر سحابة الإلكترون 10,000 مرة كُبر قطر النواة.
يكون للبروتونات والنيوترونات نفس الكتلة تقريبًا. لكن البروتون الواحد يزن أكثر من 1800 إلكترون. وتحتوي الذرات دائمًا على عددٍ متساو من البروتونات والإلكترونات، ويكون عدد البروتونات والنيوترونات عادةً هو نفسه. إن إضافة بروتون إلى النواة ينتج لنا عنصرًا جديدًا أقل وزنًا، وهذا ما تقوم به النجوم، بينما تؤدي إضافة نيوترون إلى إنتاج نظيرٍ أو نسخة أثقل وزنًا من ذلك العنصر.
نواة الذرة
اكتُشفت النواة في عام 1911 من قبل عالم الفيزياء النيوزيلندي، رذرفورد، الذي اقترح في عام 1920 إطلاق اسم البروتون على الجزيئات ذات الشحنة الإيجابية في النواة. ونظريًا قال رذرفورد أن هناك جسيمًا محايدًا داخل النواة، وتمكن تلميذه جيمس تشادويك عالم الفيزياء البريطاني من تأكيد ذلك عام 1932.
تقريبًا كل كتلة الذرة موجودة في نواتها. يكون للبروتونات والنيوترونات الكتلة نفسها تقريبًا «البروتون أقل قليلًا» وتمتلك نفس الزخم الزاوي وفقًا لمختبر لورنس بيركلي الوطني.
تلتحم مكونات النواة مع بعضها بواسطة (القوة النووية القوية)،إحدى القوى الأساسية الأربع في الطبيعة. وتتغلب هذه القوة بين البروتونات والنيوترونات على قوة التنافر الكهربائية، والتي وفقًا لقواعد الكهرباء، من شأنها أن تُبعد البروتونات عن بعضها. بعض الأنوية الذرية غير مستقرة لأن قوى الربط تختلف باختلاف الذرات بناءً على حجم النواة. ثم تتحلل هذه الذرات إلى عناصر أخرى، مثل تحلل الكربون 14 إلى نيتروجين 14.
البروتونات

البروتونات هي جزيئات موجبة الشحنة موجودة داخل نواة الذرة. اكتشفها رذرفورد في تجاربه على أنابيب أشعة الكاثود التي أجراها بين عامي 1911 و1919. البروتونات أقل كتلة من النيوترونات فهي ذات كتلة نسبية = 0.9986 (بالمقارنة لو اعتبرنا أن كتلة النيوترون =1) أو حوالي 1.673×10-27 كيلوغرام.
عدد البروتونات في الذرة يحدد نوع العنصر.على سبيل المثال، تمتلك ذرة الكربون 6 بروتونات، والهيدروجين 1، والأكسجين 8. يُطلق على عدد البروتونات في الذرة بالعدد الذري للعنصر، وعدد البروتونات يحدد أيضًا السلوك الكيميائي للعنصر. يُرتب الجدول الدوري العناصر وفقًا لعددها الذري.
يتكون كل بروتون من 3 كواركات -كواركين صاعدين (لكل منهما شحنة موجبة قدرها ⅔) وكوارك للأسفل (شحنته سالبة قدرها ⅓)- يتم جمعها معًا بواسطة جسيمات دون ذرية أخرى تدعى الغلونات، وهي عديمة الكتلة.
الإلكترونات في الذرة

الإلكترون صغير مقارنة بالبروتونات والنيوترونات، فهو أصغر منها بأكثر من 1800 مرة. لو اعتبرنا أن كتلة النيوترون =1 فإن الكتلة النسبية للإلكترون = 0.0005439 أو حوالي 9.109×10-31 كيلوغرام.
اكتشف عالم الفيزياء البريطاني طومسون، الإلكترون في عام 1887، والمعروفة أصلًا بـ”Corpuscles” أي الكريات، والإلكترونات سالبة الشحنة وتنجذب كهربائيًا للبروتونات موجبة الشحنة. تحيط الإلكترونات بالنواة في مسارات تسمى المدارات، وهي فكرة طرحها عالم الفيزياء النمساوي شرودنجر، في عشرينيات القرن المنصرم. يعرف هذا النموذج اليوم بالنموذج الكمومي أو نموذج السحابة الإلكترونية. تكون المدارات الداخلية القريبة من النواة كروية أما المدارات الخارجية أكثر تعقيدًا بكثير.
إن التوزيع الإلكتروني هو الوصف المداري لمواقع الإلكترونات في ذرة نموذجية. باستخدام التوزيع الإلكتروني ومبادئ الفيزياء، يمكن للكيميائيين التنبؤ بخصائص الذرة. مثل الاستقرار ونقطة الغليان والتوصيل.
الإلكترون الخارجي هو ما يهم على الأغلب في مجال الكيمياء. غالبًا ما يتم اختصار تدوين الوصف المداري الطويل للأغلفة الإلكترونية واستبدالها برمز لغاز نبيل بين قوسين. طريقة الكتابة هذه تبسط كثيرًا وصف الجزيئات الكبيرة.
على سبيل المثال، التوزيع الإلكتروني للبريليوم (Be) هو 1s^22s^2. لكن يكتب اختصارًا He] 2s^2]. الـ[He] يعادل جميع مدارات الإلكترونات في ذرة الهيليوم. والحروف s,p,d,f تحدد شكل المدارات ويوضح الحرف العلوي عدد الإلكترونات في ذلك المدار. ويحتوي اليورانيوم، كمثال أخر على التوزيع الإلكتروني:
1s^22s^22p^63s^23p^64s^23d^104p^65s^24d^105p^66s^2 4f^145d^106p^67s^25f^4
والذي يمكن اختصاره إلىRN] 7s^25f^4].
النيوترونات

يستخدم النيوترون كمقارنة لحساب الكتلة النسبية للبروتونات والإلكترونات (حيث يكون له كتلة نسبية قدرها 1) وله كتلة فيزيائية تبلغ 1.6749×10-27 كيلوغرام.
اكتُشفت النيوترونات نظريًا من قبل رذرفورد في عام 1920. والاكتشاف الحقيقي لها كان من نصيب تشادويك في عام 1932. تم اكتشاف النيوترونات خلال التجارب عندما أُطلقت الذرات على ورقة رقيقة من البريليوم؛ إذ انطلقت جسيمات دون ذرية عديمة الشحنة، كانت النيوترونات.
النيوترونات جسيمات عديمة الشحنة موجودة في جميع الأنوية الذرية «باستثناء هيدروجين1». تكون كتلة النيوترون أكبر قليلًا من كتلة البروتون. ومثل البروتونات، النيوترونات مكونة أيضًا من كواركات -كوارك واحد متجه للأعلى (مع شحنة موجبة ⅔) وكواركين للأسفل (لكل منهما شحنة سالبة ⅓).
ما الفرق بين ذرات النظائر المختلفة للعناصر؟
يمكنك مشاهدة فيديو لشرح النظائر من موقع Live Science عبر الضغط هنا
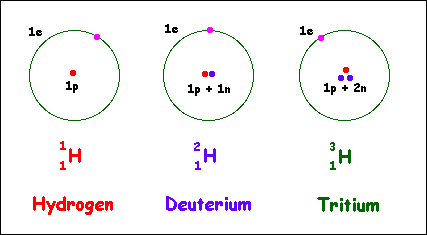
يحدد عدد النيوترونات في نواة الذرة نظير ذلك العنصر. مثلًا، للهيدروجين 3 نظائر معروفة: البروتيوم، والديوتيريوم، والتريتيوم. البروتيوم يرمز إليه 1H وهو الهيدروجين العادي؛ لديه 1بروتون و1 إلكترون وليس لديه نيوترونات. يحتوي الديوتيريوم (D أو 2H) على 1 بروتون، 1 إلكترون و1 نيوترون. ويحتوي التريتيوم (Tأو 3H) على 1 بروتون، 1 إلكترون، و2 نيوترون.
تاريخ الذرة
يعود تاريخ نظرية الذرة إلى العام 440 قبل الميلاد للعالم والفيلسوف اليوناني (ديموقريطوس). على الأرجح أن ديموقريطوس بنى نظريته حول الذرة على أعمال فلاسفة سابقين إذ وفقًا لـ( أندرو ج.فان ميلسن- Andrew G.VanMelsen) مؤلف كتاب “From Atomos to Atom”: كان مفهوم الذرة معروفًا لبارمينيدس معلم ديموقريطوس إذ اقترح مبدأ الهوية.
هذا المبدأ الذي ينص على أن “كل الكينونات تجتمع لتشكل الوجود” ساعد فلاسفة آخرين، من ضمنهم ديموقريطوس، لمواصلة أعمالهم ووضع النظرية الذرية في نهاية المطاف.
إن شرح ديموقريطوس للذرة يبدأ بحجر. هذا الحجر إن قسمناه يعطينا نصفين من نفس الحجر. وإذا كسرناه بشكل مستمر فسوف نصل إلى قطعة صغيرة للغاية لايمكن كسرها بعد ذلك. يأتي مصطلح (ذرة) من الكلمة اليونانية «غير قابلة للتجزئة»، والتي خلص ديموقريطوس إلى أنها النقطة التي لا يمكن عندها تقسيم أي نوع من المادة.
وتضمن تفسيره أفكارًا تقول بأن الذرات موجودة بشكلٍ منفصل عن بعضها، وأن كمية الذرات لا حصر لها وأنها تتحرك ويمكن أن تتحد مع بعضها لتكوين مادةٍ ما لكن لا تتحول إلى ذرات جديدة، وأنه لا يمكن تقسيمها. ومع ذلك، لأن معظم الفلاسفة آنذاك -خاصةً أرسطو ذا السلطة النافذة- اعتقدوا أن كل المواد نشأت من الأرض والهواء والنار والماء، وُضعت نظرية ديموقريطوس الذرية جانبًا.
وفقًا لقسم الكيمياء في جامعة بوردو، اعتمد الكيميائي البريطاني جون دالتون على أفكار ديموقريطوس في عام 1803 عندما طرح نظريته الذرية. احتوت نظرية دالتون العديد من أفكار ديموقريطوس، مثل أن الذرات غير قابلةٍ للتجزئة وأن الذرات المختلفة تتجمع معًا لتكوين كل المواد.
تضمنت إضافات دالتون على النظرية أفكارًا مفادها أن جميع ذرات عنصر معين تكون متماثلة وأن ذرات عنصر ما سيكون لها أوزان وخصائص مختلفة عن ذرات عنصر آخر، وأنه لا يمكن إنشاء الذرات أو تدميرها، والذرات المُشكلة للمادة لها أعداد كاملة وبسيطة.
وفقًا لمؤسسة التراث الكيميائي، اكتشف طومسون عالم الفيزياء البريطاني الإلكترون في عام 1897 وأثبت أن الذرات يمكن تقسيمها. وكان قادرًا على تحديد وجود جزيئات سالبة الشحنة من خلال دراسة خصائص التفريغ الكهربائي في أنابيب أشعة الكاثود.
ووفقًا لوثيقة طومسون عام 1897 فإن الأشعة انحرفت داخل الأنبوب، ما أثبت أن هناك شيئًا يملك شحنة سالبة داخل الأنبوب. وفي عام 1899 نشر وصفًا لنسخته عن الذرة والمعروفة بنموذج “plum pudding”. تضمن نموذج طومسون عددًا كبيرًا من الإلكترونات المعلقة في شيء موجب الشحنة ما أعطى الذرة شحنة متعادلة بشكل عام.
أما العالم الذي طور وعدل على النموذج الذري فكان رذرفورد الذي تعلم من طومسون وفقًا لقسم الكيمياء في جامعة بوردو. وفي عام 1911 نشر رذرفورد نموذجه عن الذرة الذي تضمن نواة موجبة الشحنة تدور حولها إلكترونات، ظهر هذا النموذج عندما أطلق رذرفورد ومساعدوه جسيمات ألفا على صفيحة رقيقة من الذهب. ووفقًا لمختبر جيفرسون، يتكون جسيم ألفا من بروتونين ونيوترونين وجميعها ملتحمة بالقوة النووية القوية التي تربط أي نواة.
لاحظ العلماء أن نسبة قليلة من جسيمات ألفا تنتشر في زوايا بعيدة جدًا عن الاتجاه الأساسي للحركة، بينما تمر أغلبها مباشرة. وكان رذرفورد قادرًا على تقدير حجم نواة ذرة الذهب، ووجد أن حجمها أصغر بمقدار 10,000 مرة على الأقل من حجم الذرة بأكملها وأغلب حجم الذرة هو عبارة عن فراغ. لا يزال نموذجه عن الذرة هو النموذج الأساسي الذي الذي يُستخدم اليوم.
قام عدد من العلماء الآخرين بتحسين النموذج الذري، بمن فيهم نيلز بور (اعتمد على نموذج رذرفورد ليشمل خصائص الإلكترونات في طيف الهيدروجين، وإروين شرودنجر (طور النموذج الكمومي للذرة).
وويرنير هايزنبيرغ (قال بأنه لا يمكن معرفة موضع الإلكترون وسرعته في آن واحد)، وموراي جيل مان وجورج زويغ (طوّرا بشكل مستقل النظرية القائلة بأن كل من البروتونات والنيوترونات تتكون من كواركات).
تشكلت الذرات بعد الانفجار الكبير أي قبل 13.7 مليار سنة. وعندما بدأ الكون الحار والكثيف جدًا بالتوسع أصبح أكثر برودة، وعندها سمحت الظروف بتكون الكواركات والإلكترونات. تجمعت الكواركات معًا لتشكيل البروتونات والنيوترونات، ودُمجت هذه الجسيمات في النواة. حدث هذا كله خلال الدقائق القليلة الأولى من نشأة الكون، وفقًا لـ”CERN”.

استغرق الكون 380,000 سنة حتى يبرد بدرجةٍ كافية لإبطاء الإلكترونات حتى تتمكن الأنوية من التقاطها لتشكيل أولى الذرات. وكانت أول الذرات هي الهيدروجين والهيليوم، اللذان لا يزالان أكثر العناصر وفرةً في الكون. ثم بدأت الجاذبية تسيطرعلى سُحب الغاز لتُشكل النجوم التي قامت بدورها بتشكيل ذرات أثقل (ولا تزال هذه العملية مستمرة إلى اليوم) وعند موت النجم ينفجر في حدث هائل يدعى بـ(المستعر الأعظم – Supernova)، ناشرًا محتواه الثمين في أرجاء الكون.
الجزيئات الذرية (مكونات الذرة)
البروتونات والنيوترونات أثقل من الإلكترونات وتستقر في النواة التي هي مركز الذرة. الإلكترونات خفيفة الوزن للغاية وتوجد في سحابة تدور حول النواة. يبلغ نصف قطر سحابة الإلكترون 10,000 مرة كُبر قطر النواة.
يكون للبروتونات والنيوترونات نفس الكتلة تقريبًا. لكن البروتون الواحد يزن أكثر من 1800 إلكترون. وتحتوي الذرات دائمًا على عددٍ متساو من البروتونات والإلكترونات، ويكون عدد البروتونات والنيوترونات عادةً هو نفسه. إن إضافة بروتون إلى النواة ينتج لنا عنصرًا جديدًا أقل وزنًا، وهذا ما تقوم به النجوم، بينما تؤدي إضافة نيوترون إلى إنتاج نظيرٍ أو نسخة أثقل وزنًا من ذلك العنصر.
نواة الذرة
اكتُشفت النواة في عام 1911 من قبل عالم الفيزياء النيوزيلندي، رذرفورد، الذي اقترح في عام 1920 إطلاق اسم البروتون على الجزيئات ذات الشحنة الإيجابية في النواة. ونظريًا قال رذرفورد أن هناك جسيمًا محايدًا داخل النواة، وتمكن تلميذه جيمس تشادويك عالم الفيزياء البريطاني من تأكيد ذلك عام 1932.
تقريبًا كل كتلة الذرة موجودة في نواتها. يكون للبروتونات والنيوترونات الكتلة نفسها تقريبًا «البروتون أقل قليلًا» وتمتلك نفس الزخم الزاوي وفقًا لمختبر لورنس بيركلي الوطني.
تلتحم مكونات النواة مع بعضها بواسطة (القوة النووية القوية)،إحدى القوى الأساسية الأربع في الطبيعة. وتتغلب هذه القوة بين البروتونات والنيوترونات على قوة التنافر الكهربائية، والتي وفقًا لقواعد الكهرباء، من شأنها أن تُبعد البروتونات عن بعضها. بعض الأنوية الذرية غير مستقرة لأن قوى الربط تختلف باختلاف الذرات بناءً على حجم النواة. ثم تتحلل هذه الذرات إلى عناصر أخرى، مثل تحلل الكربون 14 إلى نيتروجين 14.
البروتونات

البروتونات هي جزيئات موجبة الشحنة موجودة داخل نواة الذرة. اكتشفها رذرفورد في تجاربه على أنابيب أشعة الكاثود التي أجراها بين عامي 1911 و1919. البروتونات أقل كتلة من النيوترونات فهي ذات كتلة نسبية = 0.9986 (بالمقارنة لو اعتبرنا أن كتلة النيوترون =1) أو حوالي 1.673×10-27 كيلوغرام.
عدد البروتونات في الذرة يحدد نوع العنصر.على سبيل المثال، تمتلك ذرة الكربون 6 بروتونات، والهيدروجين 1، والأكسجين 8. يُطلق على عدد البروتونات في الذرة بالعدد الذري للعنصر، وعدد البروتونات يحدد أيضًا السلوك الكيميائي للعنصر. يُرتب الجدول الدوري العناصر وفقًا لعددها الذري.
يتكون كل بروتون من 3 كواركات -كواركين صاعدين (لكل منهما شحنة موجبة قدرها ⅔) وكوارك للأسفل (شحنته سالبة قدرها ⅓)- يتم جمعها معًا بواسطة جسيمات دون ذرية أخرى تدعى الغلونات، وهي عديمة الكتلة.
الإلكترونات في الذرة

الإلكترون صغير مقارنة بالبروتونات والنيوترونات، فهو أصغر منها بأكثر من 1800 مرة. لو اعتبرنا أن كتلة النيوترون =1 فإن الكتلة النسبية للإلكترون = 0.0005439 أو حوالي 9.109×10-31 كيلوغرام.
اكتشف عالم الفيزياء البريطاني طومسون، الإلكترون في عام 1887، والمعروفة أصلًا بـ”Corpuscles” أي الكريات، والإلكترونات سالبة الشحنة وتنجذب كهربائيًا للبروتونات موجبة الشحنة. تحيط الإلكترونات بالنواة في مسارات تسمى المدارات، وهي فكرة طرحها عالم الفيزياء النمساوي شرودنجر، في عشرينيات القرن المنصرم. يعرف هذا النموذج اليوم بالنموذج الكمومي أو نموذج السحابة الإلكترونية. تكون المدارات الداخلية القريبة من النواة كروية أما المدارات الخارجية أكثر تعقيدًا بكثير.
إن التوزيع الإلكتروني هو الوصف المداري لمواقع الإلكترونات في ذرة نموذجية. باستخدام التوزيع الإلكتروني ومبادئ الفيزياء، يمكن للكيميائيين التنبؤ بخصائص الذرة. مثل الاستقرار ونقطة الغليان والتوصيل.
الإلكترون الخارجي هو ما يهم على الأغلب في مجال الكيمياء. غالبًا ما يتم اختصار تدوين الوصف المداري الطويل للأغلفة الإلكترونية واستبدالها برمز لغاز نبيل بين قوسين. طريقة الكتابة هذه تبسط كثيرًا وصف الجزيئات الكبيرة.
على سبيل المثال، التوزيع الإلكتروني للبريليوم (Be) هو 1s^22s^2. لكن يكتب اختصارًا He] 2s^2]. الـ[He] يعادل جميع مدارات الإلكترونات في ذرة الهيليوم. والحروف s,p,d,f تحدد شكل المدارات ويوضح الحرف العلوي عدد الإلكترونات في ذلك المدار. ويحتوي اليورانيوم، كمثال أخر على التوزيع الإلكتروني:
1s^22s^22p^63s^23p^64s^23d^104p^65s^24d^105p^66s^2 4f^145d^106p^67s^25f^4
والذي يمكن اختصاره إلىRN] 7s^25f^4].
النيوترونات

يستخدم النيوترون كمقارنة لحساب الكتلة النسبية للبروتونات والإلكترونات (حيث يكون له كتلة نسبية قدرها 1) وله كتلة فيزيائية تبلغ 1.6749×10-27 كيلوغرام.
اكتُشفت النيوترونات نظريًا من قبل رذرفورد في عام 1920. والاكتشاف الحقيقي لها كان من نصيب تشادويك في عام 1932. تم اكتشاف النيوترونات خلال التجارب عندما أُطلقت الذرات على ورقة رقيقة من البريليوم؛ إذ انطلقت جسيمات دون ذرية عديمة الشحنة، كانت النيوترونات.
النيوترونات جسيمات عديمة الشحنة موجودة في جميع الأنوية الذرية «باستثناء هيدروجين1». تكون كتلة النيوترون أكبر قليلًا من كتلة البروتون. ومثل البروتونات، النيوترونات مكونة أيضًا من كواركات -كوارك واحد متجه للأعلى (مع شحنة موجبة ⅔) وكواركين للأسفل (لكل منهما شحنة سالبة ⅓).
ما الفرق بين ذرات النظائر المختلفة للعناصر؟
يمكنك مشاهدة فيديو لشرح النظائر من موقع Live Science عبر الضغط هنا

يحدد عدد النيوترونات في نواة الذرة نظير ذلك العنصر. مثلًا، للهيدروجين 3 نظائر معروفة: البروتيوم، والديوتيريوم، والتريتيوم. البروتيوم يرمز إليه 1H وهو الهيدروجين العادي؛ لديه 1بروتون و1 إلكترون وليس لديه نيوترونات. يحتوي الديوتيريوم (D أو 2H) على 1 بروتون، 1 إلكترون و1 نيوترون. ويحتوي التريتيوم (Tأو 3H) على 1 بروتون، 1 إلكترون، و2 نيوترون.
تاريخ الذرة
يعود تاريخ نظرية الذرة إلى العام 440 قبل الميلاد للعالم والفيلسوف اليوناني (ديموقريطوس). على الأرجح أن ديموقريطوس بنى نظريته حول الذرة على أعمال فلاسفة سابقين إذ وفقًا لـ( أندرو ج.فان ميلسن- Andrew G.VanMelsen) مؤلف كتاب “From Atomos to Atom”: كان مفهوم الذرة معروفًا لبارمينيدس معلم ديموقريطوس إذ اقترح مبدأ الهوية.
هذا المبدأ الذي ينص على أن “كل الكينونات تجتمع لتشكل الوجود” ساعد فلاسفة آخرين، من ضمنهم ديموقريطوس، لمواصلة أعمالهم ووضع النظرية الذرية في نهاية المطاف.
إن شرح ديموقريطوس للذرة يبدأ بحجر. هذا الحجر إن قسمناه يعطينا نصفين من نفس الحجر. وإذا كسرناه بشكل مستمر فسوف نصل إلى قطعة صغيرة للغاية لايمكن كسرها بعد ذلك. يأتي مصطلح (ذرة) من الكلمة اليونانية «غير قابلة للتجزئة»، والتي خلص ديموقريطوس إلى أنها النقطة التي لا يمكن عندها تقسيم أي نوع من المادة.
وتضمن تفسيره أفكارًا تقول بأن الذرات موجودة بشكلٍ منفصل عن بعضها، وأن كمية الذرات لا حصر لها وأنها تتحرك ويمكن أن تتحد مع بعضها لتكوين مادةٍ ما لكن لا تتحول إلى ذرات جديدة، وأنه لا يمكن تقسيمها. ومع ذلك، لأن معظم الفلاسفة آنذاك -خاصةً أرسطو ذا السلطة النافذة- اعتقدوا أن كل المواد نشأت من الأرض والهواء والنار والماء، وُضعت نظرية ديموقريطوس الذرية جانبًا.
وفقًا لقسم الكيمياء في جامعة بوردو، اعتمد الكيميائي البريطاني جون دالتون على أفكار ديموقريطوس في عام 1803 عندما طرح نظريته الذرية. احتوت نظرية دالتون العديد من أفكار ديموقريطوس، مثل أن الذرات غير قابلةٍ للتجزئة وأن الذرات المختلفة تتجمع معًا لتكوين كل المواد.
تضمنت إضافات دالتون على النظرية أفكارًا مفادها أن جميع ذرات عنصر معين تكون متماثلة وأن ذرات عنصر ما سيكون لها أوزان وخصائص مختلفة عن ذرات عنصر آخر، وأنه لا يمكن إنشاء الذرات أو تدميرها، والذرات المُشكلة للمادة لها أعداد كاملة وبسيطة.
وفقًا لمؤسسة التراث الكيميائي، اكتشف طومسون عالم الفيزياء البريطاني الإلكترون في عام 1897 وأثبت أن الذرات يمكن تقسيمها. وكان قادرًا على تحديد وجود جزيئات سالبة الشحنة من خلال دراسة خصائص التفريغ الكهربائي في أنابيب أشعة الكاثود.
ووفقًا لوثيقة طومسون عام 1897 فإن الأشعة انحرفت داخل الأنبوب، ما أثبت أن هناك شيئًا يملك شحنة سالبة داخل الأنبوب. وفي عام 1899 نشر وصفًا لنسخته عن الذرة والمعروفة بنموذج “plum pudding”. تضمن نموذج طومسون عددًا كبيرًا من الإلكترونات المعلقة في شيء موجب الشحنة ما أعطى الذرة شحنة متعادلة بشكل عام.
أما العالم الذي طور وعدل على النموذج الذري فكان رذرفورد الذي تعلم من طومسون وفقًا لقسم الكيمياء في جامعة بوردو. وفي عام 1911 نشر رذرفورد نموذجه عن الذرة الذي تضمن نواة موجبة الشحنة تدور حولها إلكترونات، ظهر هذا النموذج عندما أطلق رذرفورد ومساعدوه جسيمات ألفا على صفيحة رقيقة من الذهب. ووفقًا لمختبر جيفرسون، يتكون جسيم ألفا من بروتونين ونيوترونين وجميعها ملتحمة بالقوة النووية القوية التي تربط أي نواة.
لاحظ العلماء أن نسبة قليلة من جسيمات ألفا تنتشر في زوايا بعيدة جدًا عن الاتجاه الأساسي للحركة، بينما تمر أغلبها مباشرة. وكان رذرفورد قادرًا على تقدير حجم نواة ذرة الذهب، ووجد أن حجمها أصغر بمقدار 10,000 مرة على الأقل من حجم الذرة بأكملها وأغلب حجم الذرة هو عبارة عن فراغ. لا يزال نموذجه عن الذرة هو النموذج الأساسي الذي الذي يُستخدم اليوم.
قام عدد من العلماء الآخرين بتحسين النموذج الذري، بمن فيهم نيلز بور (اعتمد على نموذج رذرفورد ليشمل خصائص الإلكترونات في طيف الهيدروجين، وإروين شرودنجر (طور النموذج الكمومي للذرة).
وويرنير هايزنبيرغ (قال بأنه لا يمكن معرفة موضع الإلكترون وسرعته في آن واحد)، وموراي جيل مان وجورج زويغ (طوّرا بشكل مستقل النظرية القائلة بأن كل من البروتونات والنيوترونات تتكون من كواركات).
