ماء اكسجيني
- - -
الماء الأكسجيني
الماء الأكسجيني أو فوق أكسيد الهدروجين أهم ممثل بسيط لمركبات فوق الأكاسيد، يأخذ الأكسجين فيه درجة أكسدة (-1) وفي الماء للأكسجين درجة أكسدة (-2).
خواصه الفيزيائية
سائل شفاف لا رائحة له ولا لون، درجة انصهاره -43 ْس يمكن إعادة تبريده بسهولة من دون تجمد، درجة غليانه 150 ْس. يمكن مزجه مع الماء بنسب مختلفة، ويمكنه تشكيل بلورات هيدراتية H2O2,2H2O وهو مثل الماء يُذيب الأملاح جيداً.
الماء الأكسجيني النقي ثابت بصورة كافية ،وبوجود المعادن الثقيلة أو أيوناتها (شواردها) أو الوسطاء الفعالة للتحطيم مثل أملاح أو معقدات أو مركبات الحديد والنحاس والمنغنيز أو القلويات يتفكك إلى H2O وO2 ناشراً الحرارة وربما يتفكك مع انفجار.
يُحفظ الماء الأكسجيني في أوعية من الألمنيوم النقي، ويضاف إليه عادة بيروفوسفات الصوديوم Na4P2O7 أو قصديريت الصوديوم أو الأسيت أنيليد مثبِّتاً. المحاليل المائية للماء الأكسجيني أثبت من فوق أكسيد الهدروجين النقي ويمكن حفظها فترة طويلة.
بنيته
يأخذ فوق أكسيد الهدروجين استناداً إلى قياسات الأشعة السينية البنية الجزيئية المبيّنة في الشكل (1):
إن طاقة الرابطة O−O ت (200كيلو جول/مول) أصغر تقريباً بمرتين من طاقة الرابطة H−O ك (468كيلوجول/مول) وبسبب توزع الروابِط H−O غير المتناظر يعد الجزيء H2O2 قطبياً بصورة شديدة.
أما طول الرابطة O−O فيساوي 1.48 أنغستروم والرابطة H−O تساوي 0.95 أنغستروم والزاوية O−Ô−O تساوي 95 ْوتقع الرابطتان O−H في مستويين يصنعان زاوية تساوي120 ْ.
تحضيره
يحضر الماء الأكسجيني مخبرياً على البارد بتأثير الحموض الممدة في فوق أكسيد المعادن BaO2 أو Na2O2، ويحضر بسهولة من تفاعل حمض الكبريت الممدد مع فوق أكسيد الباريوم ويتكوَّن راسب كبريتات الباريوم.

وبترشيح الراسب المتشكل يحصل على محلول ممدد من H2O2 بتركيز قدره 5%.
أما صناعياً فيحضر بطرائق عديدة منها:
ـ التحليل الكهربائي لكبريتات الأمونيوم الحامضية NH4HSO4 أو حمض الكبريت باستعمال كثافة تيار عالية ومسـريين من البـلاتين فيتأكسد الأيون
 على المصعد متحولاً إلى أيون بِرأوكسو ثنائي الكبريتات
على المصعد متحولاً إلى أيون بِرأوكسو ثنائي الكبريتات  وينطلق الهدروجين على المهبط وفق التفاعل:
وينطلق الهدروجين على المهبط وفق التفاعل:

وبحلمهة [ر] الأيون أو حمضها الناتج يحصل على محلول مخفف من الماء الأكسجيني تركيزه 30%:
أو حمضها الناتج يحصل على محلول مخفف من الماء الأكسجيني تركيزه 30%:

ـ بأكسدة الكحول الإيزوبروبيلي.

وبالتقطير يتخلص من الأسيتون
وفي الطبيعة يتشكل الماء الأكسجيني كنواتج فاصلة أو مشابهة خلال أكسدة المركبات المعدنية بأكسجين الهواء، ويتشكل في الخلايا النباتية والحيوانية بتركيز ضعيف جداً، لأنه يتفكك بتأثير الخمائر الوسيطية مؤكسداً مركباتها العضوية.
خواصه الكيمياوية
تظهر الخواص الكيمياوية للماء الأكسجيني بفعله المؤكسد وفعله المُرجِع وبصفاته الحمضية وبدخوله في تشكيل مركبات معقدة. فمثلاً يظهر فعله المؤكسِد في مختلف الأوساط مشكلاً الماء. فمع أيونات اليوديد في وسط حمضي، على سبيل المثال، يتكوّن اليود الحر وكبريتات البوتاسيوم والماء:

ومع أيونات الكروم الثلاثي في وسط قلوي يتكوَّن أيون الكرومات الصفراء اللون:

ومع كبريتيد الرصاص الأسود يتكوَّن كبريتات الرصاص ذات اللون الأبيض والماء:

وهو يؤكسد أيونات الحديد الثنائي في وسط حمضي إلى أيونات الحديد الثلاثي ويتشكل الماء:

كما يؤكسد أيون النتريت إلى أيون النترات
إلى أيون النترات  ، وأيون الزرنيخيت
، وأيون الزرنيخيت  إلى أيون الزرنيخات
إلى أيون الزرنيخات  .
.
إن آلية أكسدة المركبات المختلفة بفوق أكسيد الهدروجين هي آلية صعبة، وفي أثناء التفاعلات يتشكل مركبات وسطية مثل OH وHO2 تتصف بخواص مؤكسدة أقوى من فوق أكسيد الهدروجين؛ ومثال هذا تفاعل فوق أكسيد الهدروجين مع أيون الحديد الثنائي التكافؤ:

وهذا المزيج المؤلف من محاليل H2O2 وأملاح الحديد Fe2+ المعروف بكاشف فينتون يستعمل لأكسدة المركبات العضوية المختلفة.
أما فعله المرجِع فيظهر في تأكسد أيون فوق الأكسيد
وتحوله إلى O2:

ففي المحاليل الأساسية يرجع أيون الحديد الثلاثي إلى أيون الحديد الثنائي:

ويرجِع أكسيدَ الفضة Ag2O مطلقاً الأكسجين والفضة المعدنية:

ويرجِع في الوسط الحمضي كثيراً من المواد المؤكسِدة مثل الكلور وماء الكلور وبرمنغنات البوتاسيوم وثنائي كرومات البوتاسيوم:
فمع ماء الكلور يتم إرجاع Cl (l) إلى Cl(-l)

ومع برمنغنات البوتاسيوم يتحول المنغنيز سباعي التكافؤ إلى ثنائي التكافؤ:

يستعمل هذا التفاعل للتحديد الكمي لفوق أكسيد الهدروجين في المحلول.
ومع ثاني كرومات البوتاسيوم البرتقالي اللون يتم إرجاع الكروم السداسي التكافؤ إلى الكروم الثلاثي التكافؤ ذي اللون الأخضر:

ويسلك الماء الأكسجيني في المحلول سلوك حمض ثنائي الوظيفة الحمضية وهو حمض ضعيف يتأين (يتشرد) في المحاليل المائية على مرحلتين وهو أكثر حموضة من الماء:

وهو- شأنه شأن الحموض - يغير لون عباد الشمس من الأزرق إلى الأحمر، في حين محاليله الممددة لا تؤثر في المشعرات.
يتفاعل الماء الأكسجيني مع القلويات مكوناً أملاحاً لهذا الحمض مثل Na2O2،BaO2 :

ويؤثر في أملاح الكربونات وينطلق غاز CO2

ويطلق على المركبات Na2O2 و BaO2 أي الأكاسيد التي تحوي الأيون (الشــاردة)

اسـم فوق أكاسـيد. وهي ذات بنية بلورية أيونية، أيوناتها الموجبة هي الأيونات المعدنية، وأيوناتها السالبة هي

وهي تعرف خاصة للمعادن القلوية M2O2 باستثناء الليتيوم، وللمعادن القلوية الترابية MO2. وعندما تتفاعل فوق الأكاسيد مع الماء يتكون هدروكسيد المعدن وماء أكسجيني. وأهم فوق الأكاسيد، عملياً، فوق أكسيد الصوديوم Na2O2 إذ يستعمل في المختبر لتحضير الأكسجين (يعرف لذلك بالحجر الأكسجيني) وفي صناعة المواد المنظفة، كما يستعمل لتخليص الهواء من غاز الكربون وتوليد الأكسجين وفقاً للتفاعل:

يستطيع الجذر

الدخول أيضاً في الحموض مكوِّناً فوق الحموض مثل فوق حمض الكبريت H2SO5 (حمض كارو)، وفوق حمض الكربون H2CO4 وفوق حمض الآزوت HNO4. ويدخل في الأسس مكوِّناً مثلاً NaOOH الذي يدعى بهيدرو فوق أكسيد الصوديوم.
أما الكشف النوعي عن الماء الأكسجيني فيظهر في تأثيره في ثاني كرومات البوتاسيوم في وسط حمضي بوجود ثنائي إيتيل الإيتر حيث تتكون طبقة الإيتر بلون فوق أكسيد الكروم CrO5 الأزرق السماوي والذي يتفكك بتماسه مع حمض الكبريت مشكلاً في الطبقة المائية الكروم الثلاثي ذا اللون الأخضر وفق ما يأتي:

الجزيء H2O2 مثل جزيء الماء H2O مانح ثنائيات إلكترونية حرة إذ يستطيع الدخول في المعقدات[ر. المعقد] فهو مرتبط معتدل مثلاً في الأيون المعقد [Fe (H2O)5(H2O2)]3+ وكذلك يستطيع تشكيل مركبات بلورية مشابهة للهيدرات وتدعى بـ بيرأوكسوهيدرات مثل:CaO2.2H2O2 ¨ K2CO3. 3H2O2 .
استعمالاته:
يُعطي فوق أكسيد الهدروجين ذو التركيز العالي الذي يتفكك على الحفاز (الوسيط) catalyst المؤكسِد مزيجاً غازياً من الأكسجين وبخار الماء الساخن الذي تصل درجة حرارته حتى 700 ْس (غاز بخاري)، والذي يستعمل وقوداً في المحركات النفاثة.
وفي الصناعة الكيمياوية يُستعمل فوق أكسيد الهدروجين مؤكسِداً، ومادة أولية للحصول على المركبات فوق الأكسيدية المعدنية ومبادراً في البلمرة، ومبيضاً للحرير والصوف والريش والفرو.
وبما يتعلق بمشكلة تلوث البيئة من مخلفات النواتج الكيمياوية فإن فوق أكسيد الهدروجين يتميز بقيمة خاصة مؤكسداً نقياً لا يشكل نواتج سامة.
فوق أكسيد الهدروجين غير سام، لكن سقوط محاليله المركزة على الجلد أو الأغشية المخاطية أو في مجاري التنفس تسبب حروقاً في هذه الأماكن.
وفي الطب يستعمل فوق أكسيد الهدروجين كأحد مستحضرات الوسائل المطهرة، ويستعمل محلوله بتركيز 3% للغسل والغرغرة عند التهاب الفم والتهاب اللوزتين وفي أمراض النساء ويستعمل أحياناً في توقيف النزيف الدموي الأنفي.
رياض حجازي
- - -
الماء الأكسجيني
الماء الأكسجيني أو فوق أكسيد الهدروجين أهم ممثل بسيط لمركبات فوق الأكاسيد، يأخذ الأكسجين فيه درجة أكسدة (-1) وفي الماء للأكسجين درجة أكسدة (-2).
خواصه الفيزيائية
سائل شفاف لا رائحة له ولا لون، درجة انصهاره -43 ْس يمكن إعادة تبريده بسهولة من دون تجمد، درجة غليانه 150 ْس. يمكن مزجه مع الماء بنسب مختلفة، ويمكنه تشكيل بلورات هيدراتية H2O2,2H2O وهو مثل الماء يُذيب الأملاح جيداً.
الماء الأكسجيني النقي ثابت بصورة كافية ،وبوجود المعادن الثقيلة أو أيوناتها (شواردها) أو الوسطاء الفعالة للتحطيم مثل أملاح أو معقدات أو مركبات الحديد والنحاس والمنغنيز أو القلويات يتفكك إلى H2O وO2 ناشراً الحرارة وربما يتفكك مع انفجار.
يُحفظ الماء الأكسجيني في أوعية من الألمنيوم النقي، ويضاف إليه عادة بيروفوسفات الصوديوم Na4P2O7 أو قصديريت الصوديوم أو الأسيت أنيليد مثبِّتاً. المحاليل المائية للماء الأكسجيني أثبت من فوق أكسيد الهدروجين النقي ويمكن حفظها فترة طويلة.
بنيته
يأخذ فوق أكسيد الهدروجين استناداً إلى قياسات الأشعة السينية البنية الجزيئية المبيّنة في الشكل (1):
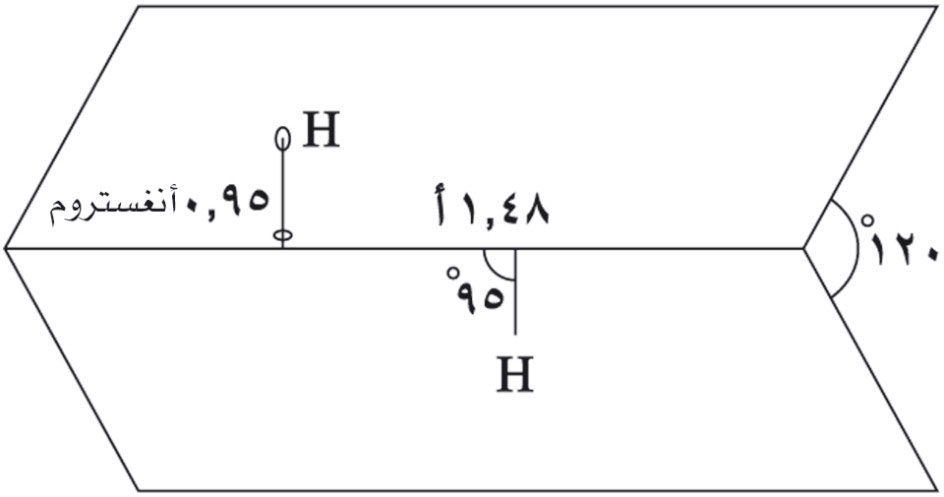 |
الشكل (1) |
أما طول الرابطة O−O فيساوي 1.48 أنغستروم والرابطة H−O تساوي 0.95 أنغستروم والزاوية O−Ô−O تساوي 95 ْوتقع الرابطتان O−H في مستويين يصنعان زاوية تساوي120 ْ.
تحضيره
يحضر الماء الأكسجيني مخبرياً على البارد بتأثير الحموض الممدة في فوق أكسيد المعادن BaO2 أو Na2O2، ويحضر بسهولة من تفاعل حمض الكبريت الممدد مع فوق أكسيد الباريوم ويتكوَّن راسب كبريتات الباريوم.

وبترشيح الراسب المتشكل يحصل على محلول ممدد من H2O2 بتركيز قدره 5%.
أما صناعياً فيحضر بطرائق عديدة منها:
ـ التحليل الكهربائي لكبريتات الأمونيوم الحامضية NH4HSO4 أو حمض الكبريت باستعمال كثافة تيار عالية ومسـريين من البـلاتين فيتأكسد الأيون
 على المصعد متحولاً إلى أيون بِرأوكسو ثنائي الكبريتات
على المصعد متحولاً إلى أيون بِرأوكسو ثنائي الكبريتات  وينطلق الهدروجين على المهبط وفق التفاعل:
وينطلق الهدروجين على المهبط وفق التفاعل:
وبحلمهة [ر] الأيون
 أو حمضها الناتج يحصل على محلول مخفف من الماء الأكسجيني تركيزه 30%:
أو حمضها الناتج يحصل على محلول مخفف من الماء الأكسجيني تركيزه 30%:
ـ بأكسدة الكحول الإيزوبروبيلي.

وبالتقطير يتخلص من الأسيتون
وفي الطبيعة يتشكل الماء الأكسجيني كنواتج فاصلة أو مشابهة خلال أكسدة المركبات المعدنية بأكسجين الهواء، ويتشكل في الخلايا النباتية والحيوانية بتركيز ضعيف جداً، لأنه يتفكك بتأثير الخمائر الوسيطية مؤكسداً مركباتها العضوية.
خواصه الكيمياوية
تظهر الخواص الكيمياوية للماء الأكسجيني بفعله المؤكسد وفعله المُرجِع وبصفاته الحمضية وبدخوله في تشكيل مركبات معقدة. فمثلاً يظهر فعله المؤكسِد في مختلف الأوساط مشكلاً الماء. فمع أيونات اليوديد في وسط حمضي، على سبيل المثال، يتكوّن اليود الحر وكبريتات البوتاسيوم والماء:

ومع أيونات الكروم الثلاثي في وسط قلوي يتكوَّن أيون الكرومات الصفراء اللون:

ومع كبريتيد الرصاص الأسود يتكوَّن كبريتات الرصاص ذات اللون الأبيض والماء:

وهو يؤكسد أيونات الحديد الثنائي في وسط حمضي إلى أيونات الحديد الثلاثي ويتشكل الماء:

كما يؤكسد أيون النتريت
 إلى أيون النترات
إلى أيون النترات  ، وأيون الزرنيخيت
، وأيون الزرنيخيت  إلى أيون الزرنيخات
إلى أيون الزرنيخات  .
.إن آلية أكسدة المركبات المختلفة بفوق أكسيد الهدروجين هي آلية صعبة، وفي أثناء التفاعلات يتشكل مركبات وسطية مثل OH وHO2 تتصف بخواص مؤكسدة أقوى من فوق أكسيد الهدروجين؛ ومثال هذا تفاعل فوق أكسيد الهدروجين مع أيون الحديد الثنائي التكافؤ:

وهذا المزيج المؤلف من محاليل H2O2 وأملاح الحديد Fe2+ المعروف بكاشف فينتون يستعمل لأكسدة المركبات العضوية المختلفة.
أما فعله المرجِع فيظهر في تأكسد أيون فوق الأكسيد

وتحوله إلى O2:

ففي المحاليل الأساسية يرجع أيون الحديد الثلاثي إلى أيون الحديد الثنائي:

ويرجِع أكسيدَ الفضة Ag2O مطلقاً الأكسجين والفضة المعدنية:

ويرجِع في الوسط الحمضي كثيراً من المواد المؤكسِدة مثل الكلور وماء الكلور وبرمنغنات البوتاسيوم وثنائي كرومات البوتاسيوم:
فمع ماء الكلور يتم إرجاع Cl (l) إلى Cl(-l)

ومع برمنغنات البوتاسيوم يتحول المنغنيز سباعي التكافؤ إلى ثنائي التكافؤ:

يستعمل هذا التفاعل للتحديد الكمي لفوق أكسيد الهدروجين في المحلول.
ومع ثاني كرومات البوتاسيوم البرتقالي اللون يتم إرجاع الكروم السداسي التكافؤ إلى الكروم الثلاثي التكافؤ ذي اللون الأخضر:

ويسلك الماء الأكسجيني في المحلول سلوك حمض ثنائي الوظيفة الحمضية وهو حمض ضعيف يتأين (يتشرد) في المحاليل المائية على مرحلتين وهو أكثر حموضة من الماء:

وهو- شأنه شأن الحموض - يغير لون عباد الشمس من الأزرق إلى الأحمر، في حين محاليله الممددة لا تؤثر في المشعرات.
يتفاعل الماء الأكسجيني مع القلويات مكوناً أملاحاً لهذا الحمض مثل Na2O2،BaO2 :

ويؤثر في أملاح الكربونات وينطلق غاز CO2

ويطلق على المركبات Na2O2 و BaO2 أي الأكاسيد التي تحوي الأيون (الشــاردة)

اسـم فوق أكاسـيد. وهي ذات بنية بلورية أيونية، أيوناتها الموجبة هي الأيونات المعدنية، وأيوناتها السالبة هي

وهي تعرف خاصة للمعادن القلوية M2O2 باستثناء الليتيوم، وللمعادن القلوية الترابية MO2. وعندما تتفاعل فوق الأكاسيد مع الماء يتكون هدروكسيد المعدن وماء أكسجيني. وأهم فوق الأكاسيد، عملياً، فوق أكسيد الصوديوم Na2O2 إذ يستعمل في المختبر لتحضير الأكسجين (يعرف لذلك بالحجر الأكسجيني) وفي صناعة المواد المنظفة، كما يستعمل لتخليص الهواء من غاز الكربون وتوليد الأكسجين وفقاً للتفاعل:

يستطيع الجذر

الدخول أيضاً في الحموض مكوِّناً فوق الحموض مثل فوق حمض الكبريت H2SO5 (حمض كارو)، وفوق حمض الكربون H2CO4 وفوق حمض الآزوت HNO4. ويدخل في الأسس مكوِّناً مثلاً NaOOH الذي يدعى بهيدرو فوق أكسيد الصوديوم.
أما الكشف النوعي عن الماء الأكسجيني فيظهر في تأثيره في ثاني كرومات البوتاسيوم في وسط حمضي بوجود ثنائي إيتيل الإيتر حيث تتكون طبقة الإيتر بلون فوق أكسيد الكروم CrO5 الأزرق السماوي والذي يتفكك بتماسه مع حمض الكبريت مشكلاً في الطبقة المائية الكروم الثلاثي ذا اللون الأخضر وفق ما يأتي:

الجزيء H2O2 مثل جزيء الماء H2O مانح ثنائيات إلكترونية حرة إذ يستطيع الدخول في المعقدات[ر. المعقد] فهو مرتبط معتدل مثلاً في الأيون المعقد [Fe (H2O)5(H2O2)]3+ وكذلك يستطيع تشكيل مركبات بلورية مشابهة للهيدرات وتدعى بـ بيرأوكسوهيدرات مثل:CaO2.2H2O2 ¨ K2CO3. 3H2O2 .
استعمالاته:
يُعطي فوق أكسيد الهدروجين ذو التركيز العالي الذي يتفكك على الحفاز (الوسيط) catalyst المؤكسِد مزيجاً غازياً من الأكسجين وبخار الماء الساخن الذي تصل درجة حرارته حتى 700 ْس (غاز بخاري)، والذي يستعمل وقوداً في المحركات النفاثة.
وفي الصناعة الكيمياوية يُستعمل فوق أكسيد الهدروجين مؤكسِداً، ومادة أولية للحصول على المركبات فوق الأكسيدية المعدنية ومبادراً في البلمرة، ومبيضاً للحرير والصوف والريش والفرو.
وبما يتعلق بمشكلة تلوث البيئة من مخلفات النواتج الكيمياوية فإن فوق أكسيد الهدروجين يتميز بقيمة خاصة مؤكسداً نقياً لا يشكل نواتج سامة.
فوق أكسيد الهدروجين غير سام، لكن سقوط محاليله المركزة على الجلد أو الأغشية المخاطية أو في مجاري التنفس تسبب حروقاً في هذه الأماكن.
وفي الطب يستعمل فوق أكسيد الهدروجين كأحد مستحضرات الوسائل المطهرة، ويستعمل محلوله بتركيز 3% للغسل والغرغرة عند التهاب الفم والتهاب اللوزتين وفي أمراض النساء ويستعمل أحياناً في توقيف النزيف الدموي الأنفي.
رياض حجازي
